研究・教育の概要
動植物や真菌類など真核生物は多彩なオルガネラを有し、その形状や機能は、周囲の状況に応じて巧みに変化します。本研究室では、代表的なオルガネラである小胞体のサイズや活性が制御され、生物が環境に適応できるメカニズムに関して、真核微生物である酵母を用いて研究しています。
強いエタノール発酵能を持つ酵母Saccharomyces cerevisiaeは、醸造や製パンやバイオエタノール製造の分野で幅広く用いられています。また、さまざまな実験を容易かつ迅速に行える酵母は、他の真核生物で起きる生命現象を研究するためのモデル生物としても利用価値が高いです。私たちの研究成果は、小胞体にダメージを与える疾病に対して細胞がどのように対処するのか理解するのに役立ちます。また、小胞体の機能を人為的に強化し、ストレスに強く有用物質の産生能が高い機能性酵母を作り出す研究も行っています。
主な研究テーマ
酵母の小胞体ストレスとUnfolded protein response (UPR)
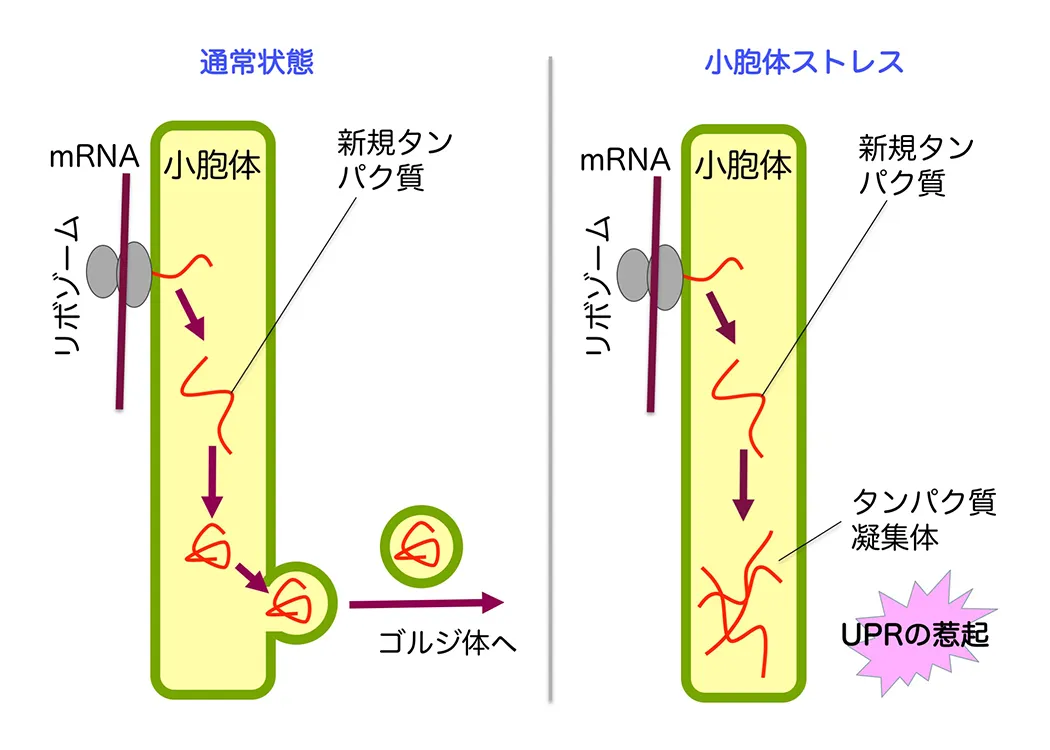
分泌タンパク質は小胞体にて折り畳まれ、完成したタンパク質のみが小胞体からゴルジ体を経て細胞表面へと運ばれます(図1左)。 また、小胞体ではさまざまな脂質類の生合成も行われます。細胞がおかれた環境が悪化すると、小胞体が機能不全を引き起こし、折り畳み不全タンパク質が小胞体に蓄積することがあります(図1右)。この状態が小胞体ストレスであり、細胞は自己防衛のため、UPRを引き起こします。
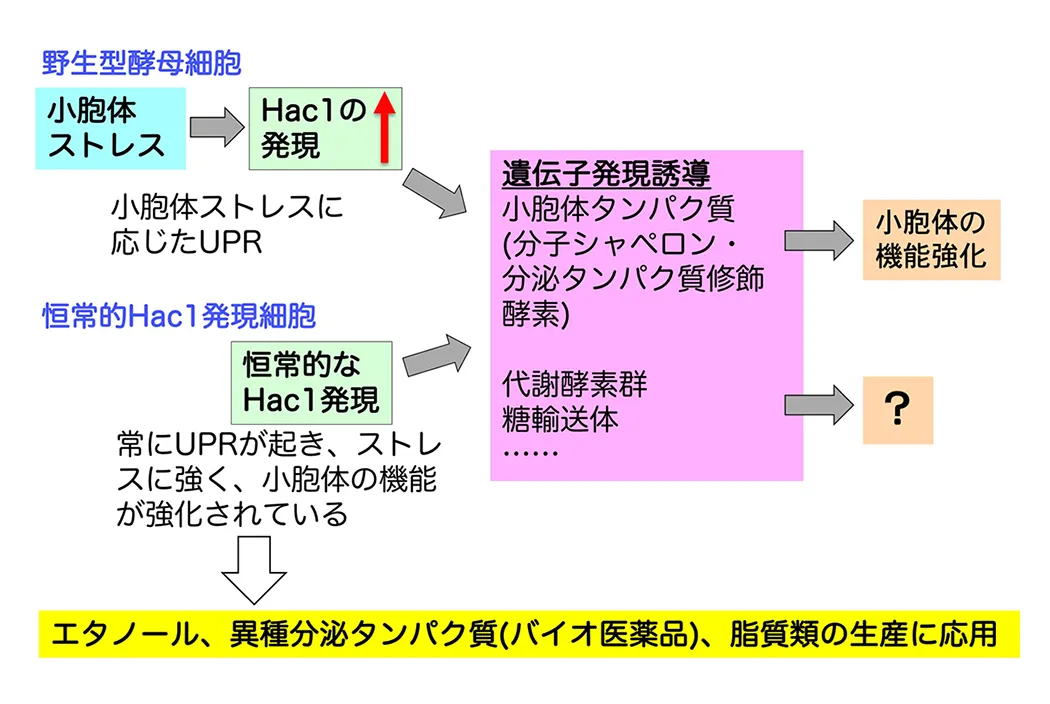
酵母のUPRでは、小胞体ストレスに応じて転写因子Hac1が作られ、小胞体で働くタンパク質をコードする遺伝子群など、数百種の遺伝子の発現が誘導されます(図2:野生型酵母)。Hac1による遺伝子発現誘導が細胞機能にどのように影響し、細胞が環境に適応するのか、その全容の解明を解明することが目標です。
小胞体を強化した酵母細胞の作出と利用
酵母にて分泌生産されたヒト由来タンパク質(サイトカインや抗体など)は、バイオ医薬品として市販されています。また、酵母を用いて油脂やテルペノイドなど脂質類を製造する技術の開発も進んでいます。これらの有用物質は小胞体にて作られるため、小胞体の強化により収量の増大が期待されます。その目的で作り出されたのが、恒常的Hac1発現細胞です(図2)。恒常的Hac1発現細胞では小胞体が伸展し、有用物質のモデルとして選んだβ-カロテンの産生量も増大していました(図3)。現在は、恒常的Hac1発現細胞に改良を加え、その実用化を目指しています。
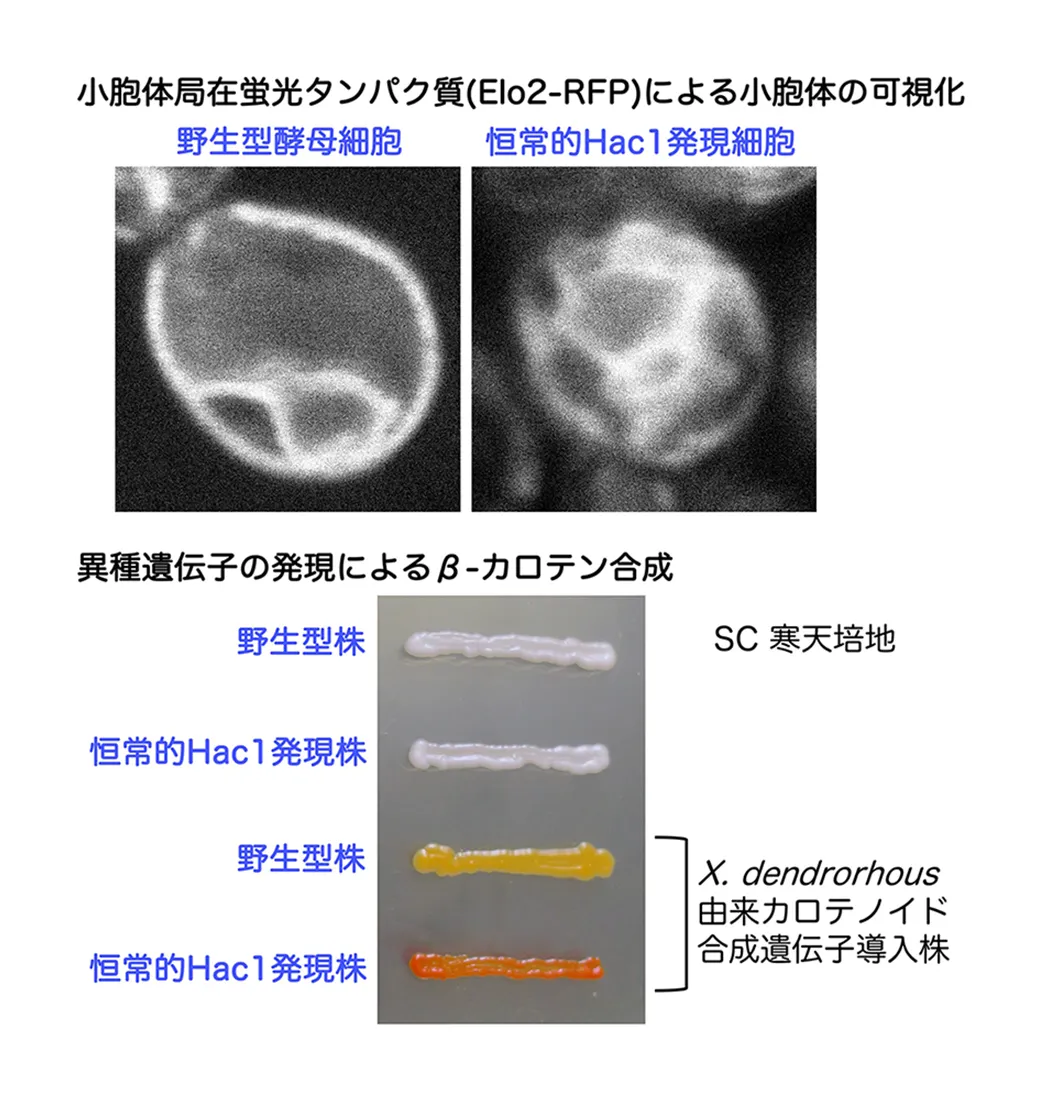
(図3) 野生型細胞に比して、恒常的Hac1発現細胞では著しく小胞体が伸展しています(上)。また、他種生物由来のカロテノイド合成遺伝子を導入したところ、野生型細胞に比して、恒常的Hac1発現細胞は多くのβ-カロテンを作り、濃く着色していました(下)。
エタノール発酵と小胞体ストレス
エタノールはタンパク質変性作用を有します。酵母でもエタノールは小胞体ストレスとなりUPRを引き起こすことが、実験室レベルの研究で分かっています。私たちは、醸造など酵母のエタノール発酵能が産業利用される局面において、小胞体ストレスやUPRがどのように関与するかを調べ、エタノール生産性の向上に役立てる計画です。
神経変性疾患の酵母での再現
小胞体ストレス時には小胞体に折り畳み不全タンパク質が蓄積しますが、サイトゾルでの病原タンパク質蓄積が小胞体ストレスとなる疾患も知られています。私たちは酵母でそのようなタンパク質を発現し、小胞体ストレス惹起メカニズムに迫ります。
耐熱酵母Kluyveromyces marxianus
生物が高温でも生き延びる術を見出すべく、50℃近い高温でも増殖可能な耐熱性酵母K. marxianusについて、UPRやその他のストレス耐性メカニズムを調べています。
 奈良先端科学技術大学院大学
奈良先端科学技術大学院大学