遺伝子発現制御(別所研究室)
-
研究室ホームページ
- https://sites.google.com/view/bessho-lab-top
-
全学オンラインセミナー
2022年度に開催されたBio Discovery Session(全学オンラインセミナー)のアーカイブ動画の一覧です。 - Bio Discovery Session
-
Webメディア
NAIST Edge BIOは、奈良先端科学技術大学院大学 バイオサイエンス領域 の各研究室で取り組んでいる「最先端」の研究プロジェクトや研究成果について、研究者だけではなく受験生や一般の方にも分かりやすく紹介するためのWebメディアです。 - NAIST Edge BIO 第15回
研究・教育の概要
脊椎動物をはじめとする多細胞生物の発生は、ダイナミックでありながら精緻に制御されたプロセスです。ゲノムにコードされた遺伝子は厳密な発現制御のもとで機能し、その結果として各細胞の性質や挙動が決定されます。さらに、細胞同士は絶えず情報を交換し、細胞数や集団の大きさ、形態といった状態を感知しながら協調的に振る舞うことで、全体として調和のとれた機能的な形態が形成されます。私たちの研究室では、マウスおよびゼブラフィッシュをモデル生物として用い、遺伝子・分子・細胞レベルにおけるこれらの動的な振る舞いを統合的に解析しています。これにより、生物を一つのシステムとして理解することを目指しています。さらに、このようなシステムの破綻によって引き起こされるさまざまな疾患の理解へとつなげることも目的としています。
主な研究テーマ
からだの繰り返し構造をつくり出す生物時計の研究
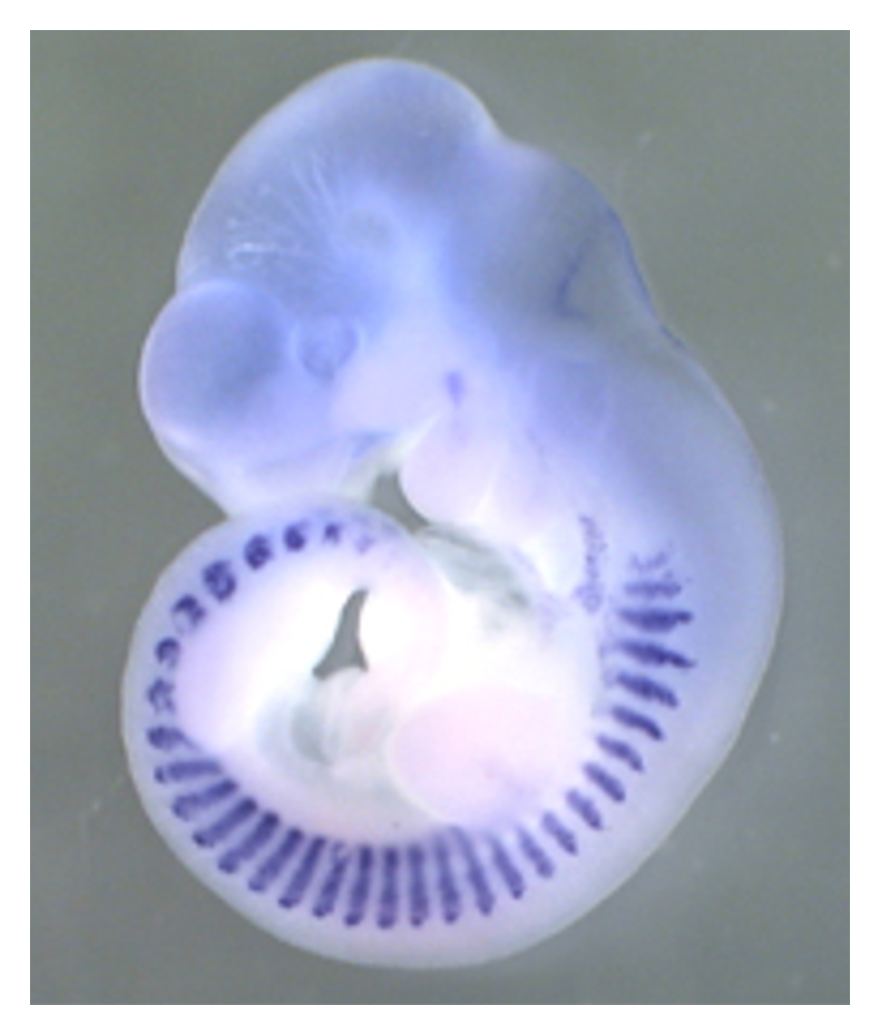
脊椎動物の発生中期に形成される「体節」は、椎骨などの繰り返し構造の基盤となる組織であり、周期的な分節化によって生じます(図2)。この周期性は、遺伝子発現の振動に基づく「分節時計」と呼ばれる生物時計によって制御されています。私たちはこれまでに、分節時計の分子メカニズムの解明に取り組んできました。分節時計は、環境変化などによって一時的に撹乱されても速やかに元の状態へ回復する、高いレジリエンスを備えたシステムです。現在は、この回復機構の解明を目指しています。さらに、遺伝子変異などによってレジリエンスが低下すると形態異常の発生率が増加すると考えられることから、本研究は先天異常の予防法の開発にもつながることが期待されます。
細胞内構造が組織、個体においてどのような役割を果たすのか、階層を横断した研究
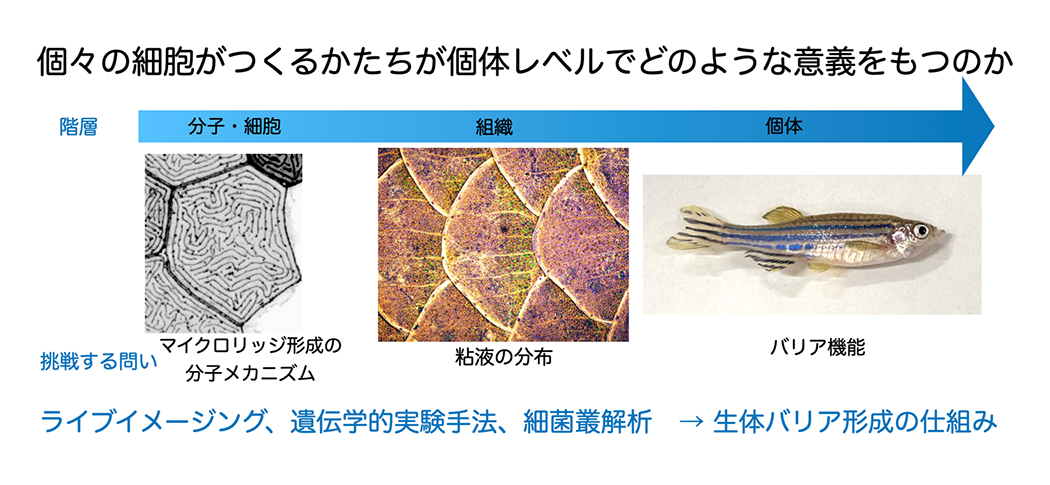
粘液は粘膜上皮において生体と体外を区別し病原体の侵入を防ぐバリアとして生体防御の最前線で重要な役割を担っています。粘膜上皮細胞に共通してみられる細胞表面から突出したひだ構造マイクロリッジは、哺乳類の角膜上皮や魚類など広く共通して見られる構造ですが形成メカニズムや機能についてよく分かっていません。ゼブラフィッシュをモデルとし遺伝学的手法やライブイメージングを用いてマイクロリッジ形成原理解明に取り組んでいます。細胞がつくる構造そのものが、組織、個体レベルでどのような役割を果たすのか、粘液分布の可視化や細菌叢解析を行い、生体バリアが形成される仕組み解明に取り組んでいます(図3)。
骨代謝における破骨細胞分化の研究
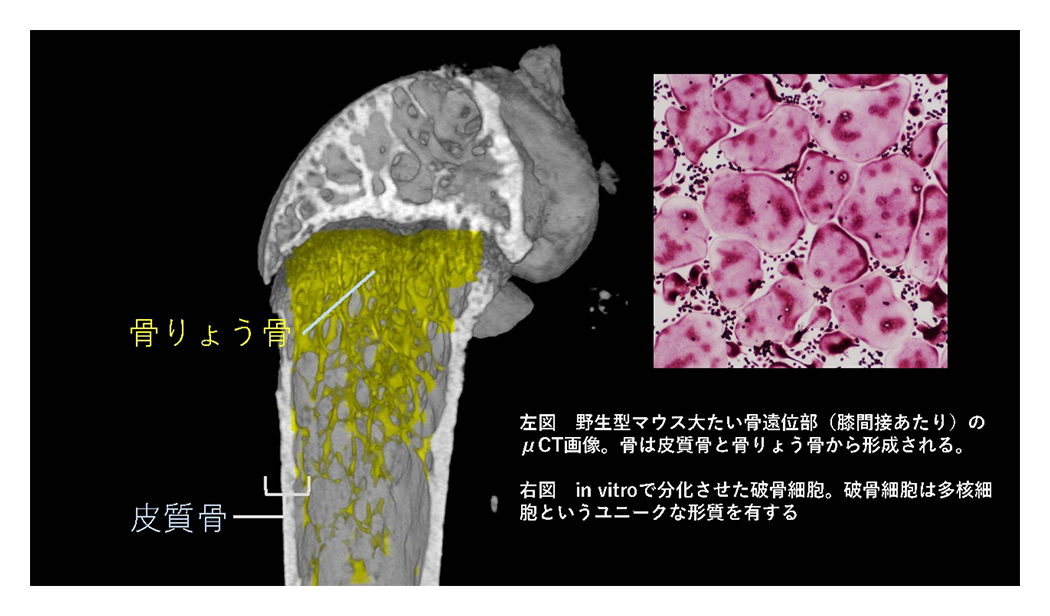
社会の高齢化が進む中で、生活の質(QOL)を高めることが重要になっています。骨粗しょう症は、年齢とともに起こりやすい病気の一つで、骨が脆くなることで骨折しやすくなります。日本では1000万人以上の人がこの病気に悩んでいます。骨は一見変わらない組織に見えますが、体の中でカルシウムなどのバランスを保つために、古い骨を壊して新しい骨をつくる働きを繰り返しています。私たちは、骨を壊す働きをもつ「破骨細胞」の分化を制御する分子メカニズムを解明し、骨疾患の治療に繋げることを目指しています(図4)。
主な発表論文・著作
- Inaba Y et al., Genes to Cells, in press, DOI: 10.1111/gtc.70101
- Ashimori A, et al., Front Neurosci, 44, 116283, 2021
- Sari DWK, et al., Scientific Reports, 8, 4335, 2018
- Akiyama R. et al., Development, 141, 1104, 2014
- Retnoaji B et al., Development, 141, 158, 2014
- Nitanda et al., FEBS J, 281, 146, 2013
- Kim W. et al., Mol Biol Cell, 22, 3541, 2011
- 別所康全, システム/制御/情報, 51, 493-498, 2007
- 別所康全, 細胞工学, 7, 755-758, 2007
(こちらのリンクはすべて外部サイトへ遷移します![]() )
)
 奈良先端科学技術大学院大学
奈良先端科学技術大学院大学