マウス体内でラットの心臓を持つキメラ動物の作製に成功
~再生臓器の移植医療への応用に新たな道拓く~
マウス体内でラットの心臓を持つキメラ動物の作製に成功
~再生臓器の移植医療への応用に新たな道拓く~
【概要】
奈良先端科学技術大学院大学(学長:塩﨑 一裕)先端科学技術研究科 バイオサイエンス領域 器官発生工学研究室の由利 俊祐客員准教授(研究当時:助教、現:国立長寿医療研究センター研究所)、有澤 範恵(研究当時:修士課程学生)、北室 皓平(修士課程学生)、磯谷 綾子准教授の研究グループは、動物の卵が受精後数日で形成する胚盤胞を用いて行う胚盤胞補完法(注1)と呼ばれる技術を使い、遺伝的に自前の心臓を持てないマウスの体内で異種のラットの多能性幹細胞(注2)由来の心臓を作り出すことに成功しました。
今回の研究では、心臓の発生に重要な遺伝子を欠損させ、心臓を作ることができなくなったマウスの初期胚を用いました。そして、その初期胚へラット多能性幹細胞を注入した後に、マウスの子宮へ移植し、胎内で発生させました。その結果、移植した初期胚から、マウス体内にラットの多能性幹細胞に由来する細胞が心臓の大部分を構成するキメラ動物(注3)を作り出すことに成功しました。
一方で、ラットの心臓を持つキメラ動物は、マウス母体内で胎生12.5日目までは確認されましたが、胎生14.5日では確認できませんでした。
この結果は、ラット由来の心臓をマウス体内で作製できますが、その心臓は発生期のある時点以降で生存に必要な機能を果たせなくなることを示唆しています。
本研究成果により、胚盤胞補完法を使って、異種の多能性幹細胞由来の心臓を作製する研究を進展させるにあたっては解決するべき問題がまだあり、この障壁を乗り越えることで、最終的には機能的な心臓ドナーの作製につながることが期待されます。
本研究は、主に、日本学術振興会(JSPS)科学研究費補助金、基盤研究B、基盤研究C、挑戦的研究(萌芽)、ノバルティス科学振興財団、奈良先端科学技術大学院大学支援財団の支援を受けて行いました。
この研究成果は、アメリカの出版社 Cell Press が発行する国際学術誌 iScience 誌 に 2024年11月17日(日)にオンライン公開され、Volume 27, Issue 12(2024年12月20日(金))に掲載されます(DOI:10.1016/j.isci.2024.111414)。
【背景と目的】
哺乳類の心臓は、血液と酸素を全身に循環させるポンプとして機能し、生命維持に必要不可欠な臓器です。しかし、成人の心筋細胞は再生能力が乏しく、虚血性心疾患が世界中でも主要な死因となっています。心臓移植は末期心不全に対する究極の治療法ですが、臓器の提供が限られており、年間約4,000~5,000 件の移植しか行われていません。そこで、ドナー不足を解決するために、動物体内でその動物の持つ発生システムを利用することで、多能性幹細胞由来の臓器を作る手法である「胚盤胞補完法」を用いた臓器作製が注目されています。しかし、過去に報告された、心臓の発生に関わる遺伝子(Nkx2.5遺伝子)の変異による心臓欠損モデルを用いた胚盤胞補完法では、心血管が多能性幹細胞由来ではない心臓が作製されました。そのため、ほとんどが多能性幹細胞由来の心臓を作製するためには、新たな心臓欠損モデルが必要とされてきました。そこで、本研究では、新たな心臓欠損モデルにより、ほとんどが異種であるラット多能性幹細胞由来となる機能を持つ心臓をマウスとラットの異種間キメラ動物体内で作製する事を目的とし、研究を始めました。
【研究成果】
まず、キメラ動物体内で野生型の細胞が心臓を構築するモデルを探索するために、「逆」胚盤胞補完法という方法によって心臓欠損モデルを評価しました。「逆」胚盤胞補完法とは、研究グループが過去に発表した論文内で開発した方法(Yuri et al., Development 151, 2024)です。まず、臓器の発生に重要な遺伝子を欠損したES細胞を作製し、次いで通常の胚盤胞補完法とは「逆」に、野生型の胚盤胞にその ES 細胞を注入し、野生型細胞と遺伝子変異細胞が入り混じるキメラ動物を作製する方法です。この方法では、全てのキメラ動物が遺伝子変異細胞と正常細胞を有することになるため、実験の効率をあげることができます。さらに、発光する赤色蛍光蛋白質で標識したES細胞を用いるので、遺伝子変異ES細胞由来の細胞分布を容易に追跡することができるという利点があります。
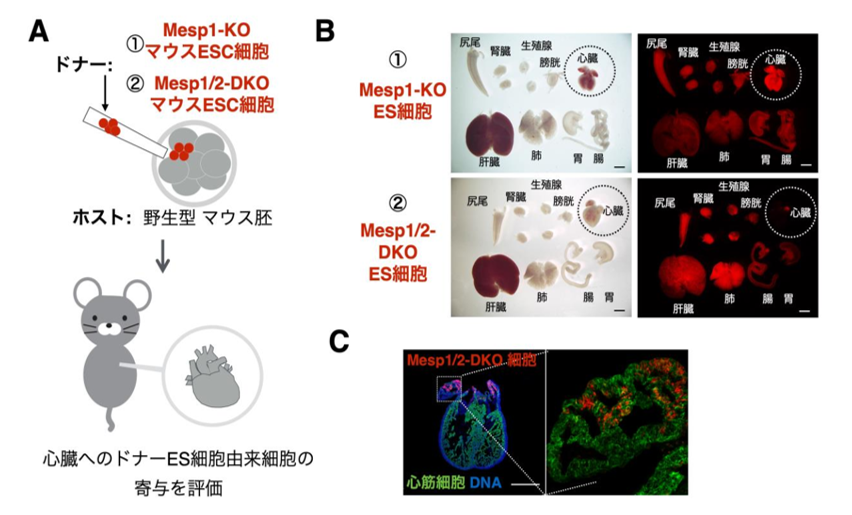
この方法を用いて、過去に心臓の発生にとって重要であるとの報告があったMesp1遺伝子欠損 (Mesp1-KO)モデルと Mesp1/Mesp2遺伝子の二重欠損 (Mesp1/2-DKO)モデルを評価しました (図 1A)。その結果、Mesp1-KO 細胞は、キメラ動物体内の心臓の形成に寄与することができたことから、Mesp1-KOモデルは野生型細胞が心臓を置換するモデルとして適さないことがわかりました(図1B)。
ところが、Mesp1/2-DKO 細胞は心房の一部には寄与しましたが、心血管を含め心室にはほとんど寄与できないことがわかりました(図1B、1C)。また、正常細胞の割合がキメラ動物に20%以上含まれるキメラ動物のみが生存し、心臓が確認されました。
すなわち、Mesp1/2遺伝子が欠損する動物体内で正常細胞が心臓を作り出すためには、キメラ動物体内に正常細胞が 20%以上含まれるという条件が必要であることがわかったのです。このキメラ動物は、生後56日間にわたり通常のマウスと同様に生存することができたことから、Mesp1/2-DKO細胞が心房の一部に存在していても、心臓の機能には影響がないことが考えられました。
次に、ラットES細胞をマウス初期胚へ注入した際に、ラット細胞がどの程度マウスの心臓へ寄与できるかを調べたところ、ラットの細胞は他の臓器と比較して、マウスの心臓組織の方へ寄与しやすく、ほとんどのキメラ個体の心臓にはラットの細胞が20%以上存在できるということがわかりました。このため、心臓を欠損するマウス初期胚を用いれば、異種間キメラ動物体内で、ラット多能性幹細胞に由来する心臓を作り出せる可能性が高いと考えました。
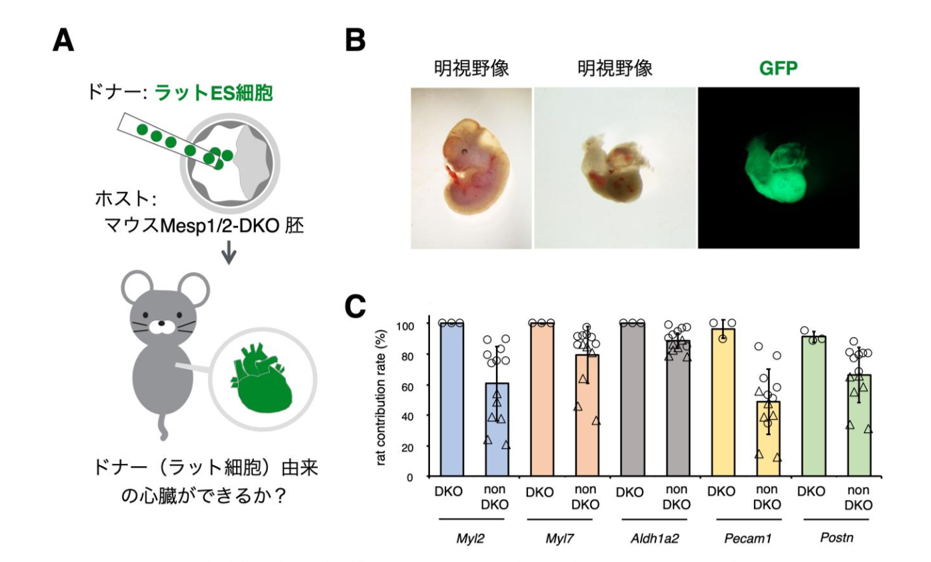
そこでMesp1/2-DKOマウスを作製し、その初期胚へラットES細胞を注入しました(図2A)。その結果、Mesp1/2-DKO 胚は心臓を持たないため胎生 8.5 日目までに致死となりましたが、ラット ES 細胞を注入した Mesp1/2-DKO 胚は、胎生8.5日目を超え、胎生12.5日目でも確認することができました(図2B)。
また、Mesp1/2-DKO胚がもつ心臓を解析したところ、心房組織や心血管も含め心臓のほとんどがラット細胞に由来することがわかりました(図2C)。つまり、この結果は、ラットの細胞がマウスの細胞よりも心房組織に寄与する能力が高いことを示すと考えられます。
以上の結果から、異種胚盤胞補完法により、マウスの体内でほとんどがラット多能性幹細胞由来の機能を持つ心臓を作り出すことができることがわかりました。一方で、このラット由来の心臓を持つ異種間キメラ動物は、胎生14.5日目までは生存しないことがわかりました。このことから、異種胚盤胞補完法で作り出されたラットの心臓は胎生8.5日目から12.5日目までは機能を持つ一方で、胎生12.5日目から14.5日目の間で生存に必要な機能を失う可能性が考えられました。


【今後の展開】
今回の研究では、異種胚盤胞補完法により、心臓欠損モデルマウスの体内でラット多能性幹細胞由来の心臓を作り出せることを明らかにしました。しかしながら、作り出された心臓は発生の過程で機能を失うことが明らかとなりました。このことから、胚盤胞補完法により、機能的な異種の心臓を作製するためには、種特異的な心臓の機能を考慮する必要性があると考えられます。機能的な心臓の作製にはさらなる研究が必要ですが、マウスとラットの異種間キメラ体内でラット多能性幹細胞由来の心臓を作れることを示せたことは、将来的に、ヒトと動物間での胚盤胞補完法による心臓作製の可能性を示すものであり、再生臓器の移植医療の発展に貢献するものと期待されます。
【用語解説】
注1 胚盤胞補完法:臓器が欠損する初期胚(胚盤胞期胚)へ多能性幹細胞を注入し、代理母の子宮へ移植することで、多能性幹細胞が、本来欠損するはずの臓器を作り出す方法。動物の発生システムを利用し、動物体内で臓器を作製するため、三次元構造を持つ多能性幹細胞由来の臓器を作製することができる。
注2 多能性幹細胞:胎盤以外の生体のどの組織にもなる能力(多能性)を持つ細胞のこと。胚性幹細胞(ES 細胞)や人工多能性幹細胞(iPS 細胞)などがある。
注3 キメラ動物:1つの個体中に2つ以上の異なる遺伝型を持つ細胞が含まれる動物のこと。
【掲載論文】
タイトル:Blastocyst Complementation-based Rat-derived Heart Generation Reveals Cardiac Anomaly Barriers to Interspecies Chimera Development
著者:由利 俊祐 1,2*,#、有澤 範恵 1,*、北室 皓平 1、磯谷 綾子 1,3#
1:奈良先端科学技術大学院大学 先端科学技術研究科 器官発生工学研究室
2:国立長寿医療研究センター研究所 研究推進基盤センター 実験動物管理室(現所属)
3:奈良先端科学技術大学院大学 生命科学研究基盤センター
*共筆頭著者 #責任著者
掲載誌:iScience
DOI:10.1016/j.isci.2024.111414
器官発生工学研究室
研究室紹介ページ:https://bsw3.naist.jp/courses/courses214.html
研究室ホームページ:https://bsw3.naist.jp/isotani/
(2024年12月06日掲載)
 奈良先端科学技術大学院大学
奈良先端科学技術大学院大学