タイショウガの成分が異常な免疫反応を抑制する仕組みを解明
~ミトコンドリアのダメージを軽減して対応~ 多様な病気の予防・治療薬の開発に期待
タイショウガの成分が異常な免疫反応を抑制する仕組みを解明
~ミトコンドリアのダメージを軽減して対応~ 多様な病気の予防・治療薬の開発に期待
【概要】
奈良先端科学技術大学院大学(学長:塩崎一裕)先端科学技術研究科 バイオサイエンス領域の織大祐助教、河合太郎教授の研究グループは、マラヤ大学(マレーシア)のNoor Hasima Nagoor(ヌアーハシマナグール)教授の研究グループとの共同研究を行い、タイショウガに含まれる1'-acetoxychavicol acetate (ACA) と呼ばれる成分が、生体防御の免疫応答である炎症に関わる特定のタンパク質複合体(NLRP3インフラマソーム) に対し、異常な活性化を抑制する働きがあることを明らかにし、その仕組みをつきとめました。このNLRP3インフラマソームは、痛風や動脈硬化などの原因になる尿酸結晶やコレステロールといった様々な病気に関係した物質によって活性化されることから創薬の標的とされ、新型コロナウイルスとの関連も指摘されています。ACAがこれらの病気の予防薬や治療薬として発展することが期待されます。
この研究成果は、国際学術誌「International Immunology(インターナショナルイミュノロジー)」に掲載されました。
【解説】
本研究で用いた1'-acetoxychavicol acetate (ACA) は、ショウガ科の植物の地下茎(図1)に含まれる成分として発見された小分子化合物です。このACAを含むショウガ科の植物として有名なのがガランガル(ナンキョウ)で、トムヤムクンやトムカーガイといった様々なアジア料理に、香辛料として用いられてきました。一方で、日本で常用されているショウガには含まれていません。
また、ガランガルは古くから伝統医薬品としても用いられており、消化器疾患やアレルギーなどに対して効果があるとされています。さらにこれまでの研究から、ACAが、抗がん作用や抗肥満効果、認知機能改善効果を示す可能性も報告されています。これらの疾患はいずれも免疫機能と密接に関連していることから、私たちの研究グループは自然免疫の観点に基づき、多彩な効果を発揮するACAが、どのようなメカニズムで効果を示すのかを解明することにより、ACAの将来的な予防薬あるいは治療薬としての利用可能性を探りました。

図1 ACAを含むショウガ科の植物の地下茎
【研究の背景と経緯】
本研究では、タイショウガに含まれる1'-acetoxychavicol acetate (ACA) と呼ばれる成分が、免疫応答において重要な炎症を起こす特定の細胞内タンパク質複合体(NLRP3インフラマソーム)の形成を抑制し、活性化が制御されていることを明らかにしました。今後、NLRP3インフラマソームが関連して発症する疾患の予防や治療のための創薬に発展することが期待されます。
インフラマソームは、主に外界に存在する異物(非自己由来の物質)を認識して免疫応答を誘導する自然免疫受容体が得た情報に基づいて細胞内で形成されるタンパク質複合体で、生体の防御機構である炎症応答の誘導に必須の分子機構です。この複合体が形成されることで、インターロイキン1βと呼ばれるサイトカイン(生理活性物質)が細胞から放出されます。インターロイキン1βは、感染症などによって誘導される炎症応答や免疫応答の誘導の他、自己免疫疾患やサイトカインストームとも密接に関係していることがよく知られています。
その中でも近年注目されているのがNLRP3インフラマソームです(図2)。NLRP3インフラマソームは、多種多様な物質によって活性化されることが報告されています。例えば、痛風や動脈硬化などの代謝性疾患の原因となる物質(尿酸結晶やコレステロールなど)やワクチンアジュバント(補助剤)として使用されているアラム(ミョウバン)、環境由来物質(アスベストなど)、さらには、インフルエンザウイルスやコロナウイルスの持つタンパク質などもNLRP3を活性化することが報告されています。これらのことから、近年、NLRP3インフラマソームは、様々な疾患の治療のための標的になる候補として注目されています。
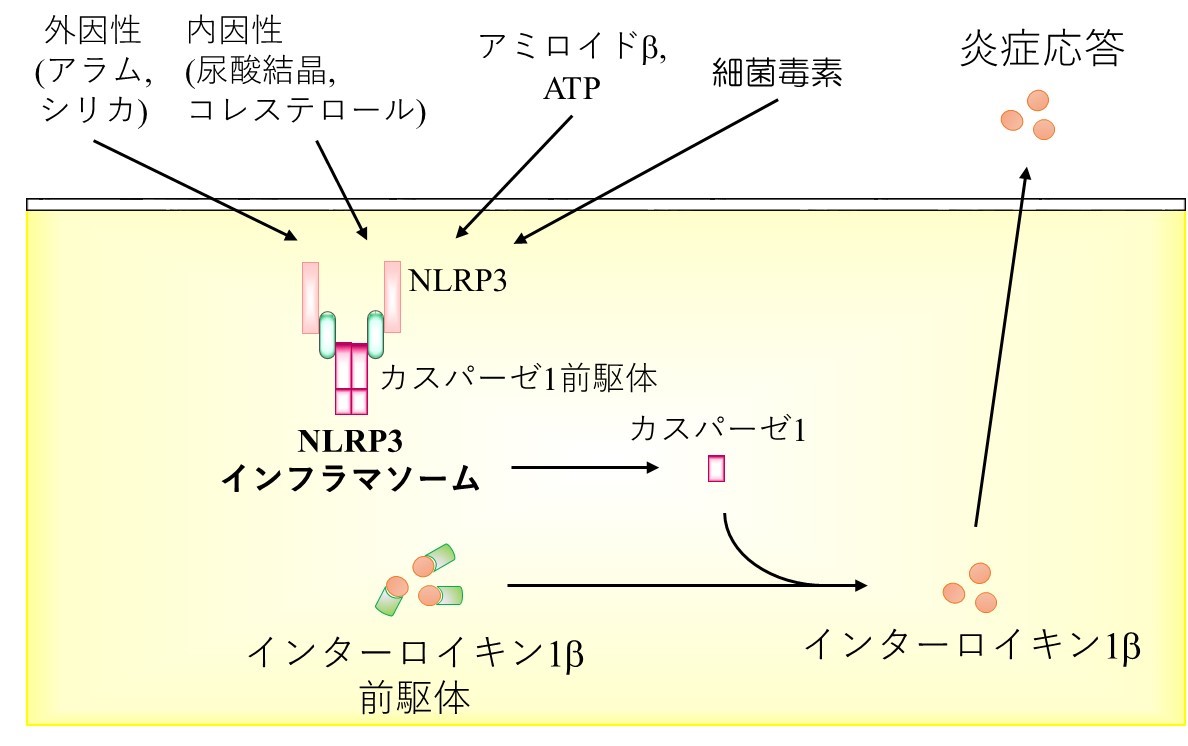
図2 NLRP3インフラマソームは様々な物質によって活性化され、炎症応答を誘導する
【研究の成果】
私たちはまず、ガランガルやACAが効果を示すとされる肥満や認知症、アレルギー、喘息などの疾患では、その病態形成にインターロイキン1βが共通して関与していることに注目しました。そこで、これらのサイトカインの放出にはインフラマソームの形成が不可欠なことから、ACAがインフラマソームの活性化を抑制することでインターロイキン1βの放出を抑制しているのではないかと考え、その検証を始めました。
まず、自然免疫応答の解析に適した免疫細胞であるマクロファージ(食細胞)をマウス骨髄細胞より作製し、その細胞の培養上清にACAを加えて前処置したのち、インフラマソームの形成とそれに続くインターロイキン1βの細胞外への放出を誘導させることができる薬剤を使って細胞を刺激しました。その結果、ACAは、培養液の上澄みに放出されるインターロイキン1βタンパク質の量を顕著に減少させることを発見しました。次に私たちは、ACAがどのような仕組みでNLRP3インフラマソームによるインターロイキン1βの放出を抑制しているのかを探りました。NLRP3インフラマソームは多種多様な分子構造が異なる物質により活性化されますが、これらの物質は共通して細胞内の小器官であるミトコンドリアにダメージを与え、その際に酸化されたミトコンドリアDNAが細胞質内に放出される現象に着目。その酸化型のDNAをNLRP3インフラマソームが感知して活発に作用するとみられることから、ACAを加えたあとにNLRP3インフラマソームを試薬で刺激して活性化した時の酸化型DNA量の変化を測定しました。
その結果、ACAは、ミトコンドリアからの酸化型DNAの放出を、刺激前の水準まで抑制していることが判明しました。こうしたことから、ACAは、ミトコンドリアで生じたダメージを軽減することにより、ミトコンドリアからの酸化型DNAの放出を抑制しており、それがNLRP3インフラマソームの活性化の抑制につながることを突き止めました(図3)。
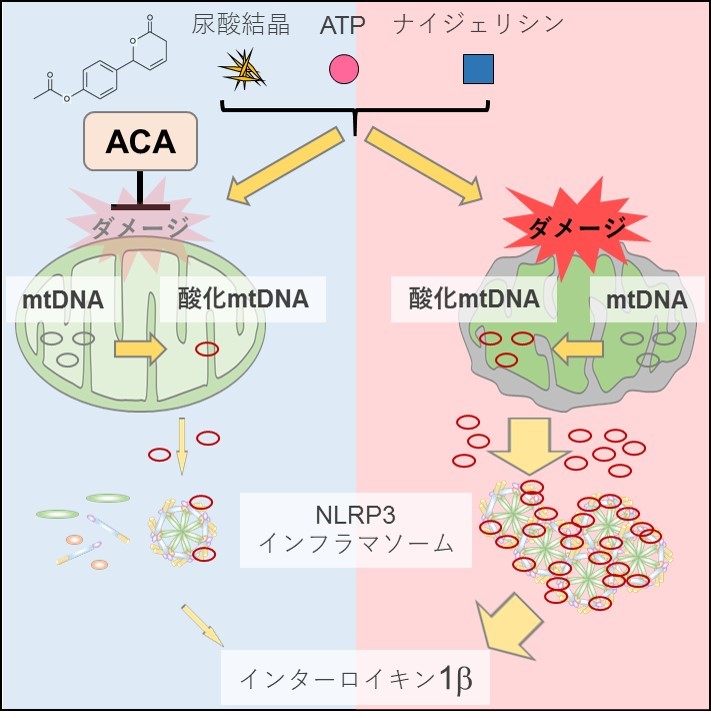
図3 ACAはミトコンドリアダメージを軽減することでNLRP3インフラマソームの活性化を抑制する
最後に、将来的な予防薬あるいは治療薬としての利用可能性を確かめるため、ACAが生体レベルでも効果を示すかどうかを、NLRP3インフラマソームが病態形成に関与するとされているマウスの腸炎モデルを用いて検証しました。マウスに腸炎を起こす薬剤を飲水投与するとともに、ACAをエサに混ぜて与えたところ、ACAを摂取したマウス群では、下痢や血便、体重減少などの症状が緩和されていただけでなく、大腸上皮細胞でのNLRP3インフラマソームの活性化も抑制されていました。これらの結果から、ACAは生体レベルでも、NLRP3インフラマソームの活性化を抑制できるということが明らかになりました。
【今後の展望】
インフラマソーム活性化の結果放出されるインターロイキン1βが病態に関与する疾患は数多く存在します。代表的なものとしては痛風やアルツハイマー型認知症などがありますが、他にもアレルギーや喘息、多発性骨髄腫、最近では、新型コロナウイルス感染症の重症化との関連も明らかになってきました。本研究では、疾患モデルとして腸炎モデルを用いてACAの効果を検証しましたが、今後は他の疾患モデルも用いてACAの効果を検証することで、新たな予防薬や治療薬の開発に繋がると期待されます。
用語解説
・自然免疫受容体
ウイルスや細菌、真菌などの構成成分を認識することで、生体への病原体の侵入を感知するセンサー。自然免疫受容体ごとに固有の対応物質(リガンド)が結合することで活性化し、炎症応答を誘導する。
・サイトカイン
細胞から細胞へと情報を伝達する小さなタンパク質。炎症を誘導する機能を持ったものは特に「炎症性サイトカイン」と総称される。他にも血球の分化・増殖を促進したり、細胞死を誘導したり、代謝に影響を与えるなど、様々なタイプがある。
・インターロイキン1β
炎症性サイトカインの一つ。生体防御に必須の炎症応答や免疫応答を誘導する機能を持つ。一方で、自己免疫疾患の病態やサイトカインストームとも深く関連している。最近では、新型コロナウイルス感染症によって起こるサイトカインストームと重症化との関連が示唆されていることから、特に注目されているサイトカインの一つである。
・マクロファージ
自然免疫系を担う代表的な細胞。食細胞として知られる。生体内で発生した代謝物や死細胞の残骸、さらには微生物を貪食することで処理する。また、初期免疫応答においても重要な役割を果たしており、免疫系の最前線で異物の侵入を感知し、サイトカインを放出することで続く免疫応答を誘導する。
・ミトコンドリア
細胞内におけるエネルギー産生の場として知られる。太古の昔に細胞に寄生した古細菌がその起源と考えられており、独自のDNAを持っている。最近では、ミトコンドリアと免疫応答との関連が注目されている。
【論文情報】
・タイトル
1′-acetoxychavicol acetate inhibits NLRP3-dependent inflammasome activation via mitochondrial ROS suppression
・著者名
Sophia P. M. Sok, Daisuke Ori, Ayana Wada, Haruna Okude, Takumi Kawasaki, Masatoshi Momota, Noor Hasima Nagoor, Taro Kawai
・雑誌
International Immunology
・DOI
10.1093/intimm/dxab016
・URL
https://academic.oup.com/intimm/advance-article/doi/10.1093/intimm/dxab016/6217095
【分子免疫制御研究室】
研究室紹介ページ:https://bsw3.naist.jp/courses/courses209.html
研究室ホームページ:https://bsw3.naist.jp/kawai/
(2021年05月10日掲載)
 奈良先端科学技術大学院大学
奈良先端科学技術大学院大学