ヒトiPS 細胞から新規誘導法を用いて脊髄損傷治療へ応用 マウス実験で回復 ~安定した分化細胞選抜、再生治療のさらなる実現に期待~
分子神経分化制御研究室の藤元祐介さん(特別研究学生) 、中島欽一教授らは、英国ケンブリッジ大学オースティンスミス教授らと共同研究で、ヒトiPS 細胞から今までとは異なる新しい方法によって誘導した神経上皮様幹細胞を脊髄損傷モデルマウスに移植し、運動機能の回復を得ることに成功しました。この成果は平成24年3月14日付けのSTEM CELLS誌オンライン版に発表された。
プレスリリース詳細(大学HP http://www.naist/ 内コンテンツ)
藤本祐介さん(特別研究学生)のコメント
今回、論文として発表することができたのは、中島教授をはじめとする研究室の方々、共著者のオースティンスミス研究室、その他多くの方々の支援おかげです。ありがとうございます。今回の研究が今後の再生治療の実現に少しでも役立つことを期待します。
中島欽一教授のコメント

研究の概要
京都大学山中伸弥教授(本学栄誉教授)らによって樹立法が開発された人工多能性幹細胞(iPS 細胞)は、体の全ての細胞に分化できる分化万能性と、分裂増殖を経てもそれを維持できる自己複製能を持ちます。免疫拒絶、倫理的問題も解決されることから、この細胞を利用した治療は脊髄損傷をはじめとする再生医療への応用が期待されています。しかし現時点では移植に必要な細胞種への誘導法や腫瘍形成の有無、機能回復の詳細なメカニズムの解明など課題や改善点が残されています。
これまでの報告では、iPS 細胞からニューロスフェア(浮遊培養してできた分化した細胞と神経幹細胞からなる球状の凝集塊)を形成させ、損傷脊髄内へ移植する方法を用いていますが、この方法では細胞の分化や手技に不安定な要素があり、塊内部に未分化なiPS 細胞が残ることで腫瘍化の原因となる可能性があります。スミス教授らは、ヒトiPS 細胞を神経幹細胞の一種である神経上皮様幹細胞へ誘導し、その際に、浮遊培養ではなく細胞を培養皿に接着させたうえ、神経系と思われる細胞のみを選別することで、均一かつ長期間神経幹細胞としての性質を維持させることができる培養法を開発しました。誘導された神経上皮様幹細胞は、ニューロスフェアを用いる場合と異なり均一な細胞であるため、さらに分化を誘導すると安定した高い割合でニューロンになり、腫瘍の発生の原因となる未分化なiPS 細胞の混入も少ないと思われます。そこで、この幹細胞をマウス脊髄損傷モデルへ移植しその効果を検討する研究を行いました。
治療を行っていないマウスの多くは体重を支えて歩けなかったのに対し、移植治療群は半分以上が体重を支えて歩けるまで回復しました。詳しく調べると、移植・生着したヒトiPS 由来細胞は、70%以上がニューロンへと分化していました。特性が異なる2種類の特殊な色素を用いて、大脳で運動をつかさどるニューロンからどのような経路で神経回路が再構築されているかを追跡してみると、移植細胞由来ニューロンがリレーするように脊髄の損傷した神経回路をつないでいる可能性が考えられました。また、もともと脊髄内に存在したニューロン(内在性ニューロン)の多くは、損傷の影響によって死滅してしまいますが、この移植によりそれが防げられることも確認されました。さらに治療後に移植細胞のみを除去すると、回復した運動機能が悪化する傾向がみられたことから、移植細胞が直接治療効果を発揮していることも分かりました。移植後3カ月まで観察しましたが腫瘍形成は認めませんでした。
今回の研究は、ヒトiPS 細胞から新たに確立された方法で誘導された神経幹細胞(神経上皮様幹細胞)を、移植治療に用いた世界初の試みであり、今後の中枢神経疾患に対する再生治療の実現に向けて重要な意義を持つと思われます。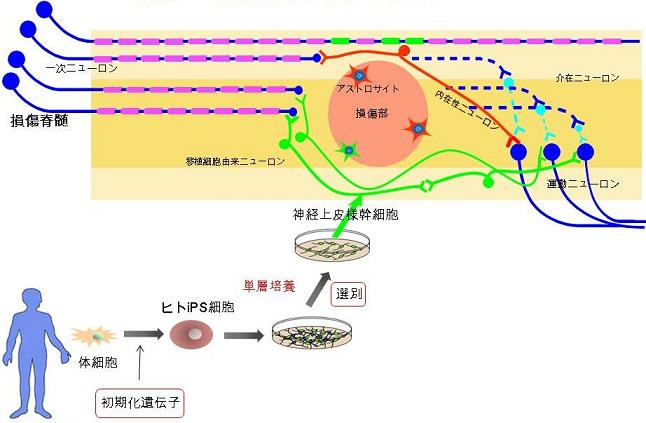
図:損傷した脊髄神経回路の再建メカニズム
(2012年03月19日掲載)
 奈良先端科学技術大学院大学
奈良先端科学技術大学院大学