2026.05.01
タンパク質を高効率で輸送可能な細胞突起からの細胞外小胞の解析
分子医学細胞生物学研究室・助教・川名 裕己
- 要旨
-
細胞外小胞(extracellular vesicles:EVs)は、細胞から放出される膜構造体であり、脂質二重膜に包まれた内部にタンパク質やRNAなどの分子を取り込んでいる。これらの小胞は細胞間で物質や情報をやり取りする手段として機能し、老化やがんを含む多様な生命現象に深く関与していることが示されている。これまでの研究では主にエンドソームを起源とする小胞が対象となってきたが、機能を保ったタンパク質を効率よく送り届けるという点では、必ずしも十分な性能を示していなかったことが指摘されている。
これに対して私たちは、細胞表面に形成される突起構造に着目し、その一部が切り離されることで生じる小胞が、細胞間で特定のタンパク質を受け渡し、受容側の細胞状態に変化をもたらす仕組みを明らかにしてきた1)。さらに最近では、この突起由来小胞に含まれるタンパク質量を定量的に評価し、それが細胞機能を変化させるのに十分な水準であることを実証した。また、突起構造に局在するタンパク質とゲノム編集酵素を融合させることで、これらの酵素を小胞内へ効率的に組み込み、標的細胞へと届けることにも成功している。加えて、詳細な比較解析により、この種の小胞は従来よく研究されてきたエンドソーム由来の小胞に比べ、タンパク質輸送の観点でより高い効率を示すことが明らかとなった2)。
本稿では、このような細胞突起に由来する細胞外小胞を活用した新たなタンパク質送達戦略について、我々の研究成果をもとに概説する。
- 主要関連論文
- 1) Nishimura T, Oyama T, Hu HT, Fujioka T, Hanawa-Suetsugu K, Ikeda K, Yamada S, Kawana H, Saigusa D, Ikeda H, Kurata R, Oono-Yakura K, Kitamata M, Kida K, Hikita T, Mizutani K, Yasuhara K, Mimori-Kiyosue Y, Oneyama C, Kurimoto K, Hosokawa Y, Aoki J, Takai Y, Arita M, Suetsugu S. (2021) Filopodium-derived vesicles produced by MIM enhance the migration of recipient cells. Developmental Cell. 56(6):842-859.e8.
doi: 10.1016/j.devcel.2021.02.029. - 2) Fujioka, T., Nishimura, T., Kawana, H., Hirosawa, K. M., Yamakawa, R., Sapili, H., Oono-Yakura, K., Nakagawa, R., Inoue, T., Nureki, O., Suzuki, K. G. N., & Suetsugu, S. (2025) Efficient cellular transformation via protein delivery through the protrusion-derived extracellular vesicles. Nature communications, 16(1), 10900.
doi:10.1038/s41467-025-66351-1
1. 細胞突起を起源とする細胞外小胞の特徴
細胞外小胞(extracellular vesicles:EVs)は、疾患に伴って量や内容物が変動することから、近年では診断指標や治療標的として注目されている。従来、EVの多くはエンドソーム系に由来し、細胞内で形成された後に細胞外へ分泌されると考えられてきた。一方、細胞膜そのものが切り出されることで生じる小胞の役割については十分に理解されていなかった。
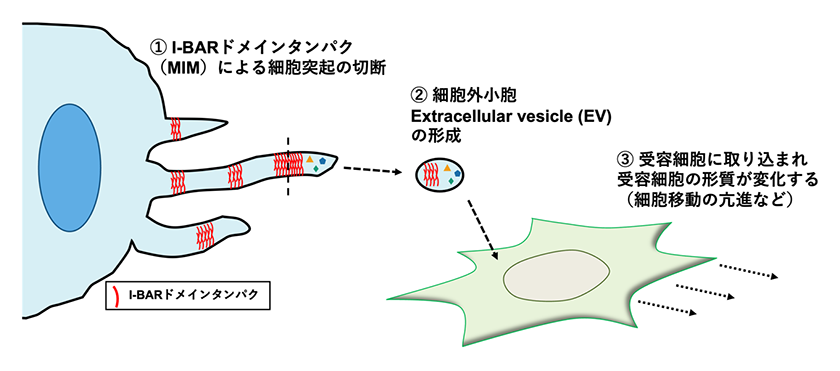
私たちは、膜変形を担うBin-Amphiphysin-Rvs(BAR)ドメインタンパク質の中でも、I-BARドメインを有する分子群に着目し、これらが細胞膜突起の形成とそこからの小胞生成を促進することを明らかにした(図1)。さらに、この経路で生じる小胞には、細胞骨格制御因子であるRac1が取り込まれており、それを受け取った細胞において運動性が変化することも見いだした。しかしながら、こうした小胞の取り込み様式や輸送能力については、当初ほとんど情報が得られていなかった。
2. 取り込み機構とタンパク質輸送能力の評価
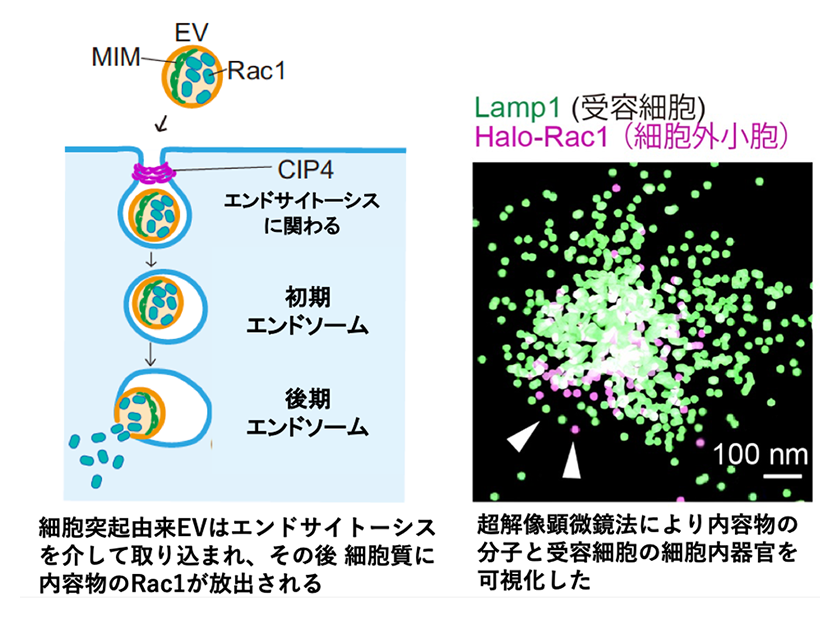
そこで本研究では、Rac1を含む細胞突起由来EVをモデルとして、受容細胞における挙動を詳細に解析した。これらの小胞を添加すると、受容細胞の移動活性が上昇することが確認されたが、この効果はエンドサイトーシス関連因子CIP4を欠損させた細胞では顕著に低下した。さらに、超解像顕微鏡を用いた観察から、これらの小胞はエンドサイトーシスによって細胞内へ取り込まれた後、エンドソームを経由して内容物を細胞質へ放出する過程をたどることが明らかとなった。
加えて、生化学的解析により輸送されるRac1の量を定量した結果、この小胞を介した送達量はマイクロインジェクションによる直接導入と同程度であることが示された。これは、細胞突起由来EVが実質的に有効なタンパク質供給手段となり得ることを示している。
3. ゲノム編集因子の輸送への応用
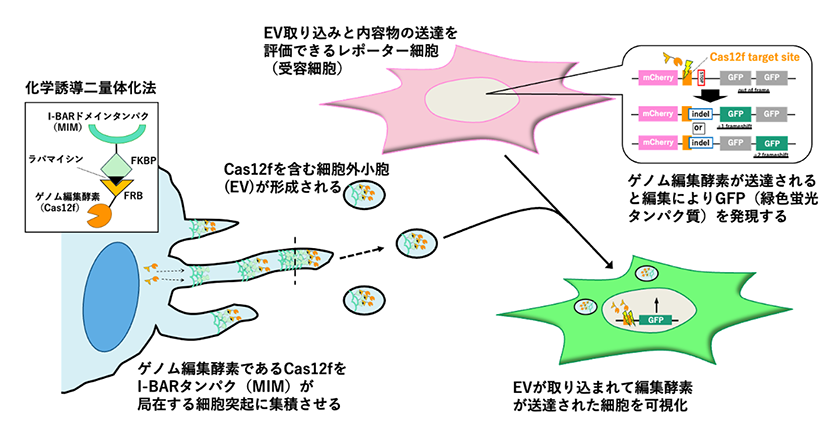
次に、この小胞の輸送能を応用する目的で、ゲノム編集酵素Cas12fおよびsgRNAの送達系を構築した(図3)。タンパク質の選択的搭載には、ラパマイシン依存的に相互作用するFRB-FKBP系を利用した。具体的には、Cas12fにFRBを融合し、細胞突起に局在するI-BARタンパク質MIMにFKBPを連結することで、両者を細胞内で会合させ、小胞内への取り込みを促進した。
この方法で得られた小胞をレポーター細胞に作用させたところ、エンドソーム由来EVを用いた場合と比較して、より高い遺伝子編集効率が得られた。また、これらの小胞は温度変化や凍結処理に対しても比較的安定であり、内部に含まれる酵素活性が維持されやすいことも確認された。
4. 今後の展望
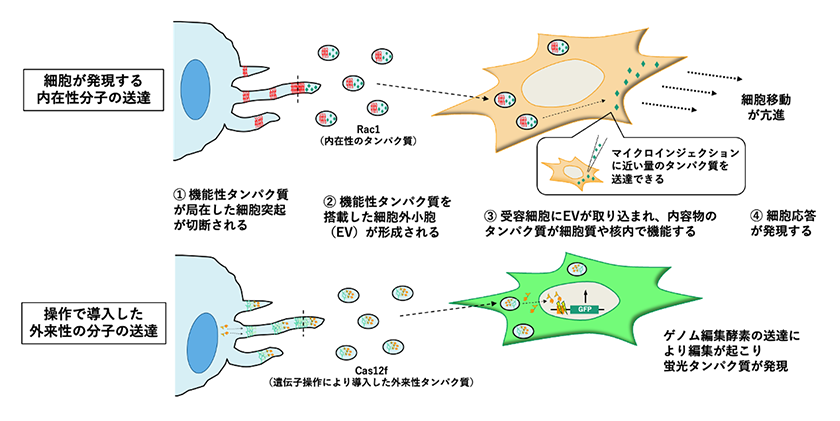
以上の結果から、細胞突起に由来するEVは、内在性タンパク質のみならず外来性タンパク質の輸送手段としても有用である可能性が示された(図4)。従来のウイルスベクターに代わる、より安全な分子送達技術としての応用が期待される。今後は、小胞への分子選別機構や標的細胞特異性の決定因子、さらには細胞内に送り込まれたタンパク質の動態制御といった点の理解を深めることで、医療応用への展開が加速すると考えられる。
参考文献
川名 裕己 NAIST Edge BIO, 0036. (2026)