| 研究内容 | スタッフ紹介 | 学生の部屋 | リンク集 | The NAISTrap Project |
atcay・HtrA1グループ
・ TGF-βシグナルを制御する遺伝子の研究
TGF-βは、初期胚の背腹軸の決定や胎児期の骨格の分化調節など、動物の形作りに必須の役割を果たしています。また、成体のさまざまな器官の機能維持にも関り、その異常は癌の悪性転化、肺繊維症や変形性関節炎など、身近な疾患の原因ともなります。私たちは、TGF-βを制御し、骨や関節の形成、関節炎の発症、癌の悪性化などに関る新しい遺伝子HtrA1を同定し、その生理機能の解析をしています。
- Tsuchiya A, Yano M, Tocharus J, Kojima H, Fukumoto M, Kawaichi M, Oka C. Expression of mouse HtrA1 serine protease in normal bone and cartilage and its upregulation in joint cartilage damaged by experimental arthritis. Bone. 2005 Sep;37(3):323-36.
・神経系の発生に関る遺伝子の研究
神経細胞の発生と機能維持にかかわる新しい遺伝子の作用機構を解析しています。その中には、晩発性アルツハイマー病の発症に関るLRP遺伝子、遺伝的小脳性運動失調症の原因となるAtcay遺伝子など、ヒトの疾患の原因となる遺伝子が含まれます。
- Shiroshima T, Oka C, Kawaichi M. Identification of LRP1B-interacting proteins and inhibition of protein kinase Calpha-phosphorylation of LRP1B by association with PICK1. FEBS Lett. 2009 Jan 5;583(1):43-8.
NMD・NAISTrapグループ
・ジーントラップ・マイクロアレイ法の開発と応用
この研究では、これまで全く別の研究手法とみなされてきた「DNAマイクロアレイ法」と「マウスES細胞を用いたランダムな遺伝子トラップ法」を機能的に融合させ、「マイクロアレイ上で興味深い発現パターンを示す遺伝子を発見した瞬間に、その遺伝子をノックアウトしたES細胞を手に入れることができる」というきわめて便利な状況を創り出すことを目指します。また、この研究の過程で、変異の起こったmRNAを選択的に破壊するNMDの機構を明らかにする糸口を得て、その研究を行っています。
- Shigeoka, T., Kawaichi, M., and Ishida, Y. Suppression of nonsense-mediated mRNA decay permits unbiased gene trapping in mouse embryonic stem cells. Nucleic Acids Res. 33, e20 (2005).
- Matsuda, E.*, Shigeoka, T.*, Iida, R., Yamanaka, S., Kawaichi, M., and Ishida, Y. (*equal contribution) Expression profiling with arrays of randomly disrupted genes in mouse embryonic stem cells leads to in vivo functional analysis. Proc. Natl. Acad. Sci. USA 101, 4170-4174 (2004).
詳しい研究内容はこちら→The National BioResource Project ;The NAISTrap Project
転写グループ
・ジーントラップ・マイクロアレイ法で破壊された遺伝子の機能解析
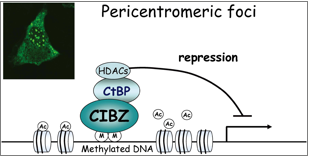
BTB ドメインを有する多くの蛋白質は細胞の発生、アポトーシス、癌化などに様々な機能を持つことが知られている。当グループは、マウス由来のBTB 転写因子 CIBZ(CtBP-interacting BTB zinc finger protein)を新規同定した。CIBZは、(a)メチル化結合タンパク質であること、(b)癌化や細胞死に重要な機能を持つCtBP (C-terminal binding protein of E1A)と結合すること、(c)転写抑制ドメインと活性化ドメインの両方を持つこと、(d)CtBP をペリセントロメアクロマチンにリクルートすることが明らかとされた (1) 。
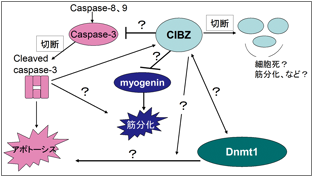
細胞が癌化するため複数の癌遺伝子と癌抑制遺伝子の変化が必要とされている。半数以上の悪性腫瘍においてp53の変異や欠失が認めており、アポトーシスが誘導しにくいのが発症の原因と考えられるが、そのメカニズムはよく分かっていない。CIBZを抑制した場合、p53に依存しないアポトーシスが亢進するということがマウスの細胞を用いて明らかとなった(2) 。
また、プロモーター領域の異常なDNAメチル化による癌抑制遺伝の不活性化も癌化の原因である。しかし、どういうメチル化結合タンパク質が関与するかなどわかっていないことも多い。従って、CIBZの機能解析によりこれらのメカニズム解明に貢献すると考えられる。
(1)Sasai Nobuhiro et al., Genes cells., 10 (9), p871-85, Sep, 2005
(2)Yu Oikawa et al., J. Biol. Chem, Vol. 283, p14242-14247, May 23, 2008
研究項目の具体例
- 酵母のTwo hybrid 系を使った遺伝子のクローニング
- In situ hybridization や免疫染色によるマウス胎児での遺伝子発現の時期と部位の解析
- 培養細胞を使った転写活性の測定
- 培養細胞のin vitro分化の系を使った遺伝子機能の解析
- 遺伝子破壊マウスによる遺伝子機能の解析
- 時期特異的に神経細胞に発現する遺伝子の単離と解析
- ES細胞とレトロウイルス・ベクターを用いたジーン・トラップ