<理想的な遺伝子トラップ法「UPATrap」の開発>

ヒトやマウスのゲノム構造が塩基配列レベルで決定された今、われわれ人類が直面する次なる難問は、「ゲノム機能の解明」です。
私たちのグループが開発した新しい遺伝子破壊法「UPATrap」は、この大目標を達成するため、欧米諸国で広く利用され始めました。
そして我が国でも、奈良先端大における私たちの研究は、昨年(2007年)より文部科学省の国家プロジェクト「ナショナルバイオリソース・プロジェクト(NBRP)」
(http://www.nbrp.jp/index.jsp)によって強力にサポートされています。このページでは、UPATrap法の開発により、それまで不可能だった一体何が可能になったのか、簡潔に解説します。
<ゲノム科学の世界的潮流>
2004年9月、国際的な共同研究計画「The Knockout Mouse Project」が発表され、遺伝子トラップと遺伝子ターゲティングの手法を組み合わせることにより、
今後5年間でマウス ES 細胞中の全遺伝子を破壊することが世界中の研究者に呼びかけられました(参考文献1)。それによれば、まずはランダムな遺伝子
トラップの手法を用い、迅速にできるだけ多くの遺伝子を ES 細胞中で破壊します。ランダムな遺伝子トラップ法で破壊できなかった遺伝子に関しては、次
のステップで、遺伝子ターゲティングの技術により一つ一つ手間ひまかけて破壊して行きます。作製された多数の変異型 ES 細胞クローンに関しては、世界
中の研究者間で自由に授受することを可能にします。
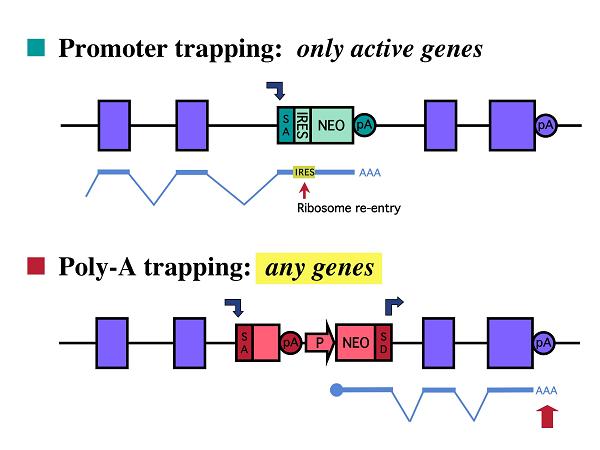
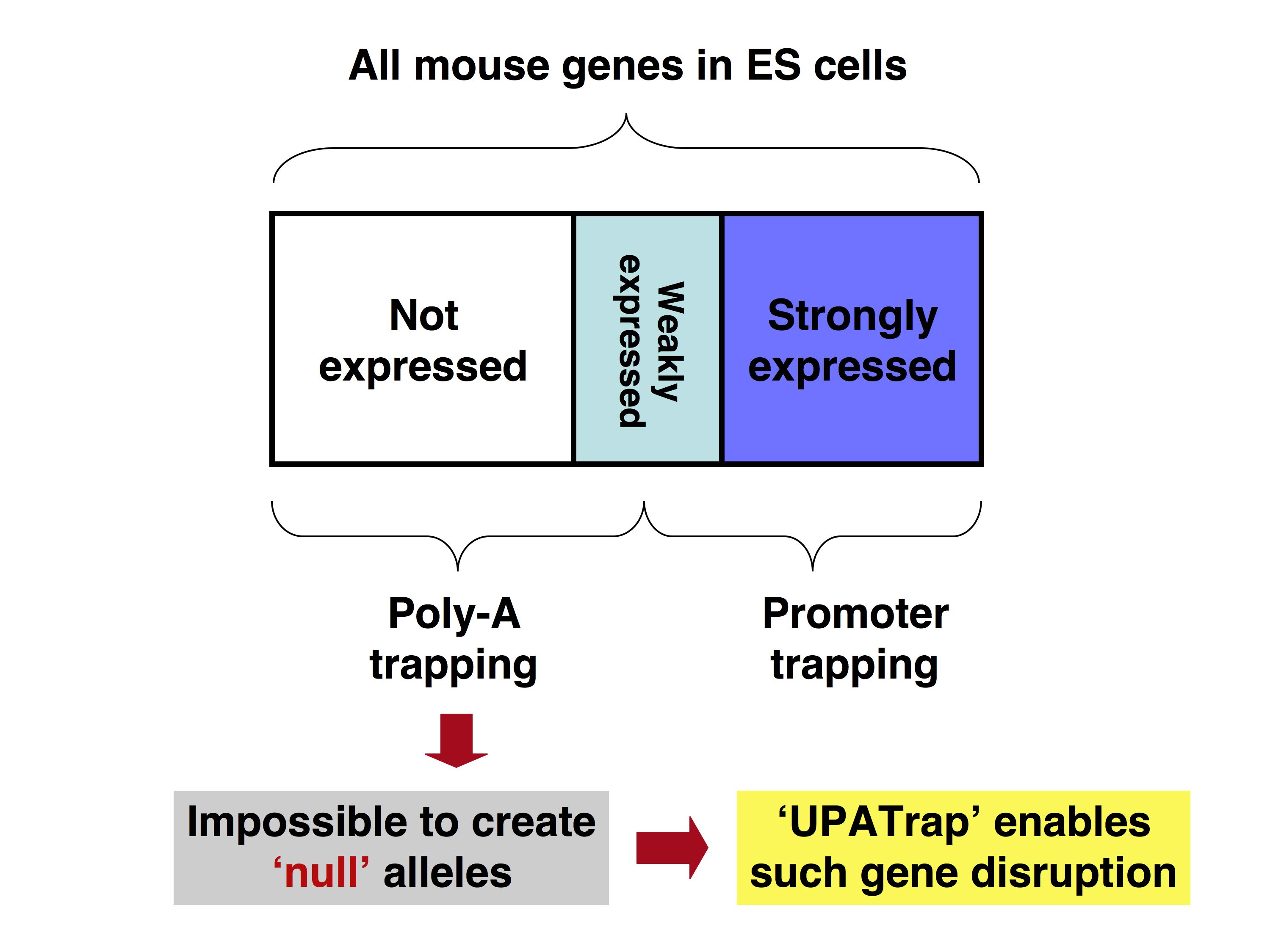
<二種類の遺伝子トラップ法>
ランダムな遺伝子トラップは、その原理に基づき、promoter trap 法と poly-A trap 法の二つに大別されます(参考文献2)。このうち、前者については
その有効性も既に十分認知されており、さまざまな分野の研究に広く応用されていますが、同法には「標的細胞中で発現されていない遺伝子をトラップする
ことができない」という致命的な欠点が存在します。これに対し、poly-A trap 法(研究業績1、2)には「標的細胞中での発現の有無にかかわらず、どのよ
うな遺伝子でも捕捉することができる」という大きなメリットが備わっていますが、実際に poly-A trap 法を用いて研究を推進しているグループは非常に少数です。

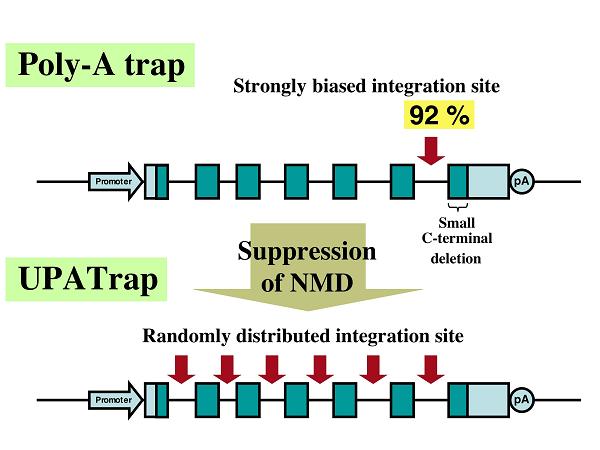
<理想的な遺伝子トラップ法「UPATrap」の開発>
最近になり私たちは、通常の poly-A trap 法ではベクターが遺伝子の最も3’側の(最後の)イントロンに挿入された細胞クローンばかりが選択的に単離されてしまう、
という事実を見出し、その分子メカニズムを解明することにも成功しました。すなわち、ベクター挿入部位に関するこの驚くべき「偏り」は、poly-A trap のために用
いられる選択マーカーの mRNA が nonsense-mediated mRNA decay (NMD、参考文献3) と呼ばれる mRNA のサーベイランス機構によって分解されてしまうために引き起こ
されていたのです(研究業績5、7、8)。さらに、理想的な遺伝子トラップ技術の確立を目指し、私たちは、選択マーカーの mRNA に対する NMD の影響を完全に排除した
新しい poly-A trap 法、「UPATrap」を開発しました(研究業績5、7、8)。この新しい遺伝子トラップ法の創出により、標的細胞中で転写活性を持たない遺伝子を、
ベクターの挿入部位に関する「偏り」が皆無の状態で捕捉することが初めて可能となりました。このことは、国際的な共同研究計画「The Knockout Mouse Project」
の遂行にとり、大きな障害となっていたステップのひとつが解消されたことを意味します。
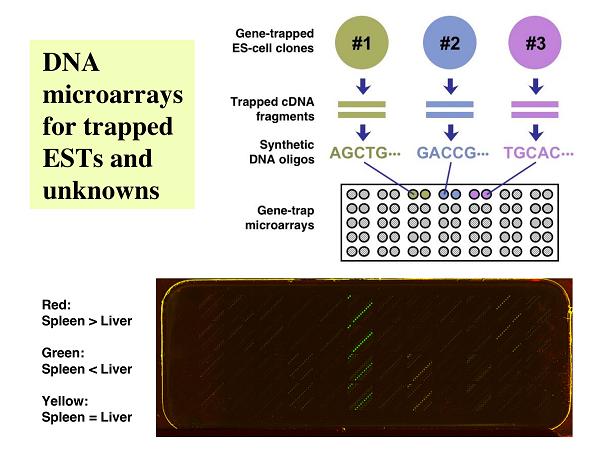
<遺伝子トラップ法と DNA マイクロアレイ技術の融合>
私たちのグループでは、数年前より「The NAISTrap Project」を展開しています(http://bsw3.naist.jp/kawaichi/naistrap-e.html)。まず、研究の第一段階では、
マウス ES 細胞中の遺伝子をpoly-A trap 型ベクターによってランダムにトラップ(破壊)します。次に、ベクターによってトラップされた遺伝子の cDNA 断片を
3’ RACE 法(特殊な PCR 技術)を用いて増幅し、その塩基配列を決定します。トラップされた遺伝子に関する情報は、「The NAISTrap Database」としてインター
ネット上で公開されています(http://bsw3.naist.jp/kawaichi/3kenfile/index.html)。通常の遺伝子トラップ法の場合、トラップされた遺伝子断片の塩基
配列を決定し、バイオインフォマティクス領域の解析を加えるところで研究は完結します。しかし、われわれの The NAISTrap Project では、トラップされた遺伝子
断片の塩基配列に基づいて独自の DNA マイクロアレイを作製し、マウスの体内におけるそれぞれの遺伝子の発現パターンを解析することにより、さらに一歩研究を
推し進めています(研究業績4)。これにより、既存の遺伝子データベースに蓄積された情報からだけでは、その「面白さ」を予測することが不可能だった全く新規の
遺伝子を同定し、直ちにその遺伝子に関するノックアウト・マウスの作製に着手することが可能になりました。
<免疫科学と神経科学>
The NAISTrap Project で使われる研究手法(新しい遺伝子トラップ法 UPATrap と DNA マイクロアレイ技術の融合)は、マウスを利用した如何なる生命科学の研究
分野にも応用可能ですが、私たちのグループでは、特に免疫科学(研究業績6)と神経科学(研究業績4)の領域の生命現象に重点を置き、研究を進めています。
参考文献
1. Austin, C. P., Battey, J. F., Bradley, A., et al. (the Comprehensive Knockout Mouse Project Consortium). The Knockout Mouse Project. Nat. Genet. 36, 921-924 (2004).
2. Stanford, W. L., Cohn, J. B. & Cordes, S. P. Gene-trap mutagenesis:
past, present and beyond. Nat. Rev. Genet. 2, 756-768 (2001).
3. Maquat, L. E. Nonsense-mediated mRNA decay: splicing, translation and mRNP dynamics. Nat. Rev. Mol. Cell Biol. 5, 89-99 (2004).
研究業績
1. Ishida, Y. & Leder, P. RET: a poly A-trap retrovirus vector for
reversible disruption and expression monitoring of genes in living cells.
Nucleic Acids Res. 27, e35 (1999).
2. Goodwin, N. C., Ishida, Y., Hartford, S., Wnek, C., Bergstrom, R. A., Leder, P., and Schimenti, J. C. DelBank: a mouse ES-cell resource for generating deletions. Nat. Genet. 28, 310-311 (2001).
3. Shimizu, J., Yamazaki, S., Takahashi, T., Ishida, Y., and Sakaguchi, S. Stimulation of CD25+CD4+ regulatory T cells through GITR breaks immunological self-tolerance. Nat. Immunol. 3, 135-142 (2002).
4. Matsuda, E.*, Shigeoka, T.*, Iida, R., Yamanaka, S., Kawaichi, M., and Ishida, Y. (*equal contribution) Expression profiling with arrays of randomly disrupted genes in mouse embryonic stem cells leads to in vivo functional analysis. Proc. Natl. Acad. Sci. USA 101, 4170-4174 (2004).
5. Shigeoka, T., Kawaichi, M., and Ishida, Y. Suppression of nonsense-mediated mRNA decay permits unbiased gene trapping in mouse embryonic stem cells. Nucleic Acids Res. 33, e20 (2005).
6. Shimizu, J.*, Iida, R.*, Sato, Y., Moriizumi, E., Nishikawa, A., and Ishida, Y. (*equal contribution) Crosslinking of CD45 on suppressive/regulatory T cells leads to the abrogation of their suppressive activity in vitro. J. Immunol. 174, 4090-4097 (2005).
7. Aiba, A., Inokuchi, K., Ishida, Y., Itohara, S., Kobayashi, K., Masu, M., Mishina, M., Miyakawa, T., Mori, H., Nakao, K., Obata, Y., Sakimura, K., Shiroishi, T., Wada, K., and Yagi, T. Mouse liaison for integrative brain research. Neurosci. Res. 58, 103-104 (2007).
8. 重岡稔章、石田靖雅. 「NMD経路の抑制による新しい遺伝子トラップシステムの構築」バイオテクノロジージャーナル(羊土社)2005年7-8月号
9. 重岡稔章、石田靖雅. 「NMD経路の抑制による理想的な遺伝子トラップシステムの構築」細胞工学(秀潤社)2005年7月号
data
受賞
1. 第2回梅園賞(重岡稔章、2005年7月15日)
2. 平成17年度・最優秀学生賞・博士課程修了者部門(重岡稔章、2006年3月24日)
3. 平成17年度・最優秀学生賞・修士課程修了者部門(井上高良、2006年3月24日)
NAISTrap メンバー
N.Ika Mayasari(D3)
Bai Jie(M2)
渡邊 司(M2)
古谷 雅(M1)
木村 優佳(NBRP実験補助員)
尾崎 綾(NBRP実験補助員)
石田 靖雅(准教授、ishiday@bs.naist.jp)