研究成果の紹介
バイオサイエンス研究科植物細胞機能研究室の橋本隆教授らが、世界初 植物の環境ストレス応答機構を解明
【概要】
植物は乾燥や高低温などの生育環境の急激な変化を瞬時に感じ取り、一時的な環境ストレスに適応できるように、細胞機能を変化させる。しかし、植物細胞が環境ストレスに対してすみやかに反応する仕組みはほとんどわかっていない。
バイオサイエンス研究科植物細胞機能研究室の橋本隆教授らの研究グループは、植物細胞の形を作り、細胞分裂で重要な働きをしている微小管という細い管状のタンパク質(生体ポリマー)が塩害による高浸透圧などの環境ストレスにさらされるとすみやかに分解される仕組みを明らかにした。
環境ストレスに反応する酵素が見つかったのは初めて。形の変化や情報の伝達などストレス対応に重要な役割をしている、と見られる。
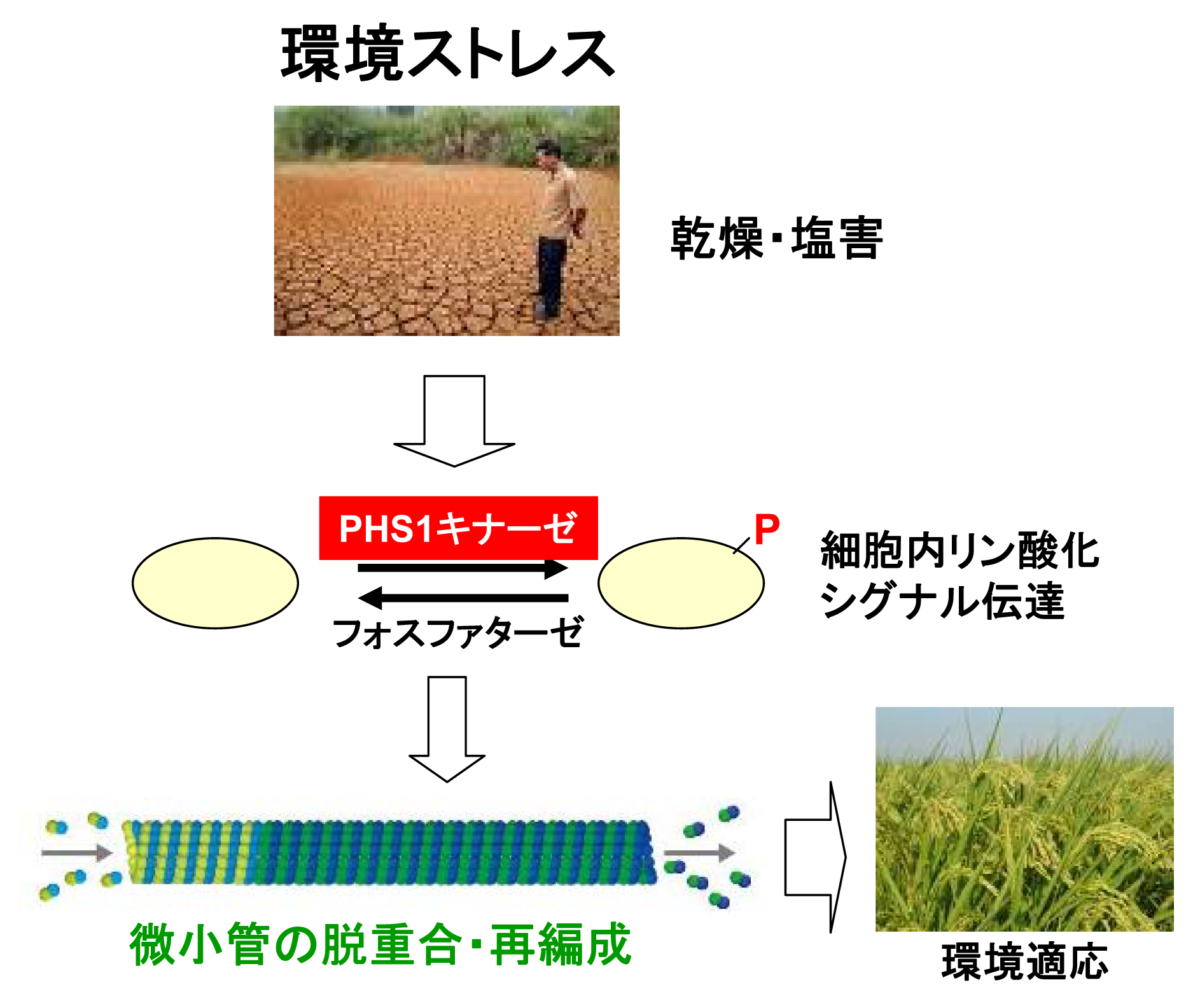
橋本教授らはシロイヌナズナを材料に微小管ポリマーの構成単位であるタンパク質(チューブリンタンパク質)をリン酸化する酵素(PHS1)を発見、PHS1は、環境ストレスにさらされると働きはじめ、その作用により微小管が短時間(30分以内)で分解することを見出した。例えば、れんが(タンパク質)で造られた家(微小管)が、形が変った(リン酸化)れんがをはめ込むことにより、ばらばらに崩壊するイメージである。
実験では、PHS1のリン酸化活性は通常は抑えられているが、植物細胞が環境ストレスに晒されるとPHS1はすみやかに活性化され、微小管ポリマーが崩壊した。
乾燥、高温、低温などの環境ストレスは作物の収量を大幅に減少させる。植物が種々の環境ストレスを感じ取り、そのシグナルを細胞の増殖や分化にすみやかに伝える仕組みを解明することにより、急激な環境変動に迅速に対応し、高収量を維持できる環境適応型作物の開発につながると期待される。
橋本隆教授のコメント
植物の微小管細胞骨格の研究は、これまで細胞周期や細胞分化に伴って骨格パ ターンがどのように変化するかという研究がほとんどであり、環境要因によって細胞骨格が再編成する現象は分子機構が全く不明であった。今回、植物細胞が高浸透圧や高塩濃度に置かれた場合に、どのようなメカニズムで微小管パターンが短時間で変化するのかを明らかにし、その際に重要な役割を果たしている植物特異的な酵素を同定した。この発見が引き金となって、植物の環境ストレス応答反応研究に、微小管細胞骨格の再編成という観点からのアプローチが期待される。
ターンがどのように変化するかという研究がほとんどであり、環境要因によって細胞骨格が再編成する現象は分子機構が全く不明であった。今回、植物細胞が高浸透圧や高塩濃度に置かれた場合に、どのようなメカニズムで微小管パターンが短時間で変化するのかを明らかにし、その際に重要な役割を果たしている植物特異的な酵素を同定した。この発見が引き金となって、植物の環境ストレス応答反応研究に、微小管細胞骨格の再編成という観点からのアプローチが期待される。
【解説】
微小管はチューブリンタンパク質が繋がって構成される筒状の生体ポリマーであり、動物、植物、酵母などの全ての真核生物で細胞分裂、細胞極性、細胞内物質輸送、などの重要な細胞機能を担っている。微小管ポリマーは細胞内では常にチューブリンが付加したり、脱離したりするために、細胞内を動き、ポリマー形状を変化させる動的なポリマーである。
今回、初めて植物細胞において微小管ポリマーが環境ストレスに迅速に反応して、チューブリンに分解される仕組みを明らかにし、その分解機能を担っている鍵因子PHS1を見出すことに成功した。高浸透圧ストレスを植物細胞に与えてから10分以内にPHS1により微小管ポリマーが一時的に分解し、ストレスを与え続けると、数時間後には微小管は元の状態に回復した。PHS1を破壊した変異株では、高浸透圧ストレスを細胞に与えても、微小管は全く反応せず、PHS1がこの環境応答に必須であることが証明された。
今後、植物の劣悪環境での生存にPHS1による微小管分解反応がどのように寄与しているのかを明らかにしてゆく必要がある。また、環境ストレスによりPHS1のリン酸化活性が活性化される仕組みを解明することも重要な研究課題である。
【論文の内容】
微小管は真核生物に高度に保存された細胞骨格であり、その高次構造、動態、他の細胞構造物との相互作用を変化させることにより、細胞分裂、細胞極性の形成、オルガネラ(構造体)の移動など多様な細胞機能に重要な役割を果たしている。
植物における微小管研究は、細胞分裂時における分裂面の決定機構並びに間期微小管が細胞伸長方向を決定する分子機構が主流を占めていた。一方で、乾燥、高低温、重金属などの劣悪環境要因が微小管をすばやく脱重合する現象がいくつかの植物種において報告されており、外来刺激に対して植物が細胞骨格の安定性をどのように制御し、環境適応しているのか興味がもたれている。しかしながら、外部シグナルに微小管が応答する分子機構は全く解明されておらず、今後の研究の発展が期待される植物科学分野のひとつである。
本論文では、モデル植物シロイヌナズナの微小管が不安定になっている優勢変異株として橋本研究室で単離され、その原因遺伝子が解明されていたpropyzamide hypersensitive 1d (phs1-d)について詳細な機能解析が行われた。PHS1は生物で高度に保存されるタンパク質リン酸化酵素(mitogen-activated protein kinase)を不活性化する脱リン酸化酵素 (MKP)に分類され、phs1-dではそのキナーゼと相互作用しているとされていたところが変異していた。シロイヌナズナ葉細胞への一過的遺伝子発現系を用いて、PHS1のどの領域に微小管不安定化能があるのかが調べられたところ、脱リン酸化触媒領域とは別の保存された機能未知の領域が植物細胞で微小管を脱重合することが判明した。さらに、この領域がαチューブリンの保存されたアミノ酸を特異的にリン酸化する新奇リン酸化活性をもつことを種々の実験で証明した。
さらにPHS1によりリン酸化されたチューブリンは微小管ポリマーに重合しないこと、植物細胞ではPHS1の脱リン酸化活性がこのチューブリンリン酸化活性を抑制していることを明らかにしている。最後に、本論文では高浸透圧や高塩濃度などの外界ストレスがPHS1を介して表層微小管の迅速な脱重合を引き起こしていることを発見し、外界ストレスがPHS1の脱リン酸化による抑制を解除することによりすばやい外来刺激応答を可能にしていると議論している。
【論文の波及効果】
外界ストレスによる微小管ポリマーの急速な消失は、植物細胞が外界環境の変化をモニタリングし、数分の時間オーダーで環境変化に対応する分子機構として注目される。本研究により発見されたPHS1シグナル伝達因子による微小管状態変化が植物細胞のどのような外界適応反応に係っているかは今後明らかにしてゆかねばならない。一方、PHS1の活性を人為的に制御することにより、環境変化により効率的に適応できる植物を育成できるかもしれない。また、PHS1活性を目に見える形で観察できる標識プローブを開発できれば、環境ストレスを数値化して定量モニタリングできる環境指標植物系統を開発できる可能性がある。
【説明図】

(2013年10月18日掲載)
