研究内容
背景:小胞体ストレスとUnfolded protein response (UPR)
小胞体は、動植物そして酵母など、あらゆる真核生物細胞が持つオルガネラです。 その実体は扁平あるいはチューブ状の形をした袋であり、細胞外に分泌されるタンパク質や他のオルガネラで働くタンパク質の製造工場として働きます。 酵母は約6千種類、高等動植物は数万種類のタンパク質を作り、その中のおよそ3割が小胞体へと運び込まれます。 小胞体の内部には複数の分子シャペロンが存在しており、小胞体に送られてきた新生タンパク質を折り畳みます。 そして、正しく折り畳まれたタンパク質のみ小胞体から運び出されるのです。 また、小胞体のもう一つの役割は、リン脂質や油脂(中性脂質)などさまざまな脂質類の生合成の場となることです。
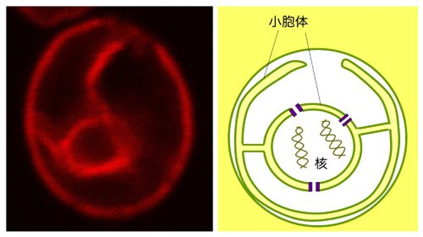
酵母細胞の小胞体
蛍光タンパク質(サンゴ由来RFP)が融合した小胞体タンパク質Elo2を発現する酵母(Saccharomyces cerevisiae)細胞
小胞体の機能不全は小胞体ストレスと呼ばれ、小胞体内への折り畳み不全タンパク質の蓄積を伴います。 異常なタンパク質の存在は小胞体ストレスとなり、認知症などを引き起こす神経変性疾患と小胞体ストレスとの関連は多くの研究者によって研究されています。 また、タンパク質の折り畳みを妨げる化学物質も小胞体ストレスになります。
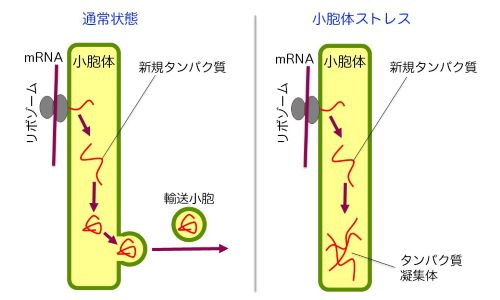
小胞体ストレス
通常状態では、リボゾームから小胞体に送り込まれたタンパク質は、分子シャペロンの補助を受けて折り畳まれた後、輸送小胞に詰め込まれ、ゴルジ体を経て細胞表面や他のオルガネラに運ばれる。 一方、小胞体ストレス状態では、折り畳まれなかったタンパク質が小胞体に蓄積し、タンパク質凝集体として細胞にダメージを与える。
小胞体ストレスに抗うための遺伝子発現変動がUnfolded Protein Response (UPR)です。小胞体ストレスに応じて、小胞体で働く分子シャペロンなどの発現が誘導され、小胞体ストレス状態が緩和されます。 動植物を含むあらゆる真核生物でUPRは引き起こされますが、そのメカニズムの解明は酵母(Saccharomyces cerevisiae)をモデル生物とした研究が先行してきました。
Ire1は小胞体ストレスセンサーとして知られている膜タンパク質です。 小胞体ストレスに応じてIre1は活性化して、RNA切断酵素として働きます。 酵母ではその標的はHAC1 mRNAです。 Ire1によってスプライシングされたHAC1 mRNAは核内転写因子タンパク質に翻訳され、UPRにおける遺伝子発現誘導を司ります。
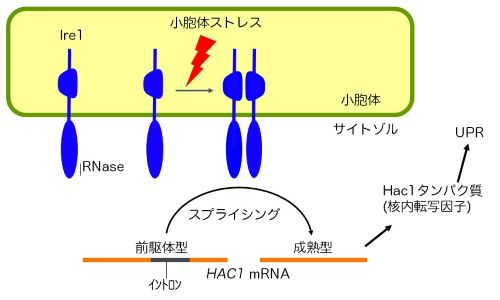
酵母のUPR
Ire1は小胞体ストレスに応じて自己会合し、RNA切断酵素(RNase)として働く。そしてHAC1 mRNAをスプライシングにより成熟させ、UPRにおける遺伝子発現変動を引き起こす。
研究成果1: 小胞体ストレスに応じたIre1の多量体化
私たちは、小胞体ストレスに応じてIre1が自己会合して巨大な多量体タンパク質を形成することを見いだしました。 Ire1多量体は強いRNA切断活性を示し、UPRを惹起します。
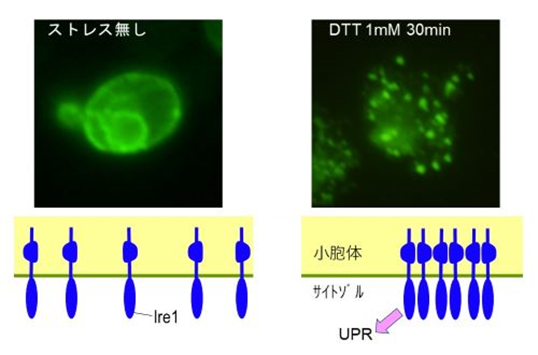
小胞体ストレスに応じたIre1の局在変化
酵母細胞内のIre1の局在を、蛍光抗体染色法によって可視化した。ストレスが無い状態ではIre1は小胞体全体に広がっているが、小胞体ストレス状態では(この場合は、DTTを培地に加え、小胞体におけるタンパク質の折り畳みを阻害した)、Ire1は大きな多量体を形成して点状の局在を示す。
研究成果2: Ire1が小胞体ストレスを感知する仕組み
小胞体ストレスセンサーとして働くIre1は、どのような仕組みで小胞体ストレスを感知するのでしょうか? 小胞体内部に蓄積した折り畳み不全タンパク質をIre1は直接的に認識して活性化することを、私たちは見いだしました。 しかし一方、膜脂質の構成成分の異常も小胞体ストレスとなり、Ire1を活性化します。 この場合のIre1活性化メカニズムは、折り畳み不全タンパク質蓄積によるものとは異なるようです。
研究成果3: どのような局面で細胞は小胞体ストレス状態になるのか?
人為的な実験室環境や遺伝子操作以外のどのような局面で細胞は小胞体ストレス状態になり、UPR経路が活性化されるのでしょうか? 私たちは酵母細胞をモデルとして、その問題にアプローチしてきました。 私たちのこれまでの研究により、現在でも環境汚染物質として世界中で問題となっているカドミウムが、小胞体におけるタンパク質の折り畳みを阻害することが明らかとなりました。 また、酵母によるエタノール発酵は産業的にも重要な事象ですが、高濃度のエタノールは小胞体ストレスとなり、エタノール発酵中の細胞障害の一因となり得ることを見いだしました。
研究成果4: 常にUPRが起きている酵母細胞の作製と応用
上述のように、小胞体ストレスに応じてIre1が多量体化して活性化し、酵母細胞ではHAC1 mRNAをスプライシングにより成熟させます。 そして、成熟型HAC1 mRNAの翻訳産物であるHac1は、UPRにおける遺伝子発現誘導を担います。 では、成熟型HAC1 mRNAをコードする遺伝子を酵母細胞に導入し、Hac1を恒常的に発現させると、どのようなことが起きるでしょうか? そのような恒常的Hac1発現酵母細胞では、外部から小胞体ストレスを与えなくても常に小胞体ストレス応答が起き、小胞体のサイズや機能が増大します。 小胞体は分泌タンパク質の折り畳みや修飾を行い、また、脂質分子の生合成を行うオルガネラです。 私たちが作製した恒常的Hac1発現酵母細胞では、分泌タンパク質や脂質類の産生量が向上することが示されました。
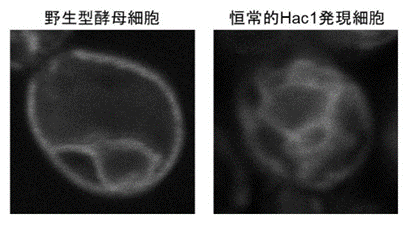
恒常的Hac1発現酵母細胞における小胞体の伸展
RFP―Elo2の発現により小胞体を可視化した細胞の蛍光顕微鏡写真

恒常的Hac1発現酵母細胞における脂質類生産の向上
酵母株に他種生物のカロテノイド合成遺伝子を導入し、寒天培地上で増殖させた。野生型酵母細胞に比べて、恒常的Hac1発現細胞は多くのβ-カロテンを生成し、濃く着色している。
これからの研究テーマ
エタノール発酵とUPRとの関わり
酵母が行うエタノール発酵は、醸造や製パン、そしてバイオエタノール製造にとって重要です。 エタノールが小胞体ストレスとなりUPRを引き起こすことは、実験室レベルの研究では分かっていますが、しかし、酵母をエタノール生産に用いる局面において、どの程度にUPRが起こっているか、そして、UPRがエタノール発酵を助けるのか阻害するのかも分かっていません。 そこで私たちの研究室は、醸造など場面でUPRをモニターし、それがどのようにエタノール生産に影響を与えるのか解明することを目指しています。
人為的にUPRを引き起こした酵母細胞を物質生産に用いる
酵母を用いて生産されたヒト由来の分泌タンパク質(ホルモン、サイトカイン、抗体断片など)は、バイオ医薬品として実用化されています。 また、現在は主として植物から作られている油脂やテルペノイドなどの脂質類を酵母にて製造することも、近い将来には可能になると期待されています。 これらの有用物質は小胞体で作られるので、恒常的Hac1発現酵母細胞を用いて小胞体の機能やサイズを向上させることにより、増産できると期待されます。 しかし、恒常的Hac1発現酵母細胞のデメリットとして、増殖の遅さが挙げられます。 私たちの研究室では、さらなる遺伝子改変を加えてこのデメリットを解決し、恒常的Hac1発現酵母細胞による物質生産を実用化することを目指しています。また、UPRにより代謝経路が変化するならば、恒常的Hac1発現酵母細胞は市場価値のある水溶性代謝産物の製造にも用いることができる可能性があります。
耐熱性酵母Kluyveromyces marxianus
酵母Kluyveromyces marxianusは、50℃近くの高温でも増殖できるという、極めてユニークな特性を有しています。高温ではタンパク質の折り畳みが阻害され、多くの生物は小胞体ストレス状態になります。私たちの研究室は、UPRについての研究を足がかりとして(また、UPR以外のことにも視野を広げて)、Kluyveromyces marxianusが高温耐性を持つ仕組みにアプローチする研究を進めます。その研究成果により、生物が高温でも育つことができる手段が見つけ出され、地球温暖化の時代に適した農業の展開に繋がるかも知れません。また、Kluyveromyces marxianusは木質系のバイオマスを利用する能力が高く、アルコール類を中心としたバイオ燃料生産のための実用化が期待されています。しかし、エタノールを含むアルコールは、小胞体ストレスを含む様々なストレスを細胞に与えます。私たちの研究室はタイの研究機関と協力し、Kluyveromyces marxianusのアルコール耐性を高め、高い収量でアルコール生産が可能な株を開発することも目指しています。
UPRは酵母細胞にどのような生理的変化を引き起こすか?
Hac1は数多くの遺伝子のプロモーターに作用し、多彩な遺伝子がUPRによって発現変動します。 小胞体局在分子シャペロンなど、小胞体で働くタンパク質をコードする遺伝子の発現誘導は、小胞体ストレスの緩和に寄与することが容易に想像できます。 しかし、なぜHac1の標的になるのか分からない遺伝子も多く、酵母細胞がUPRを起こしてから小胞体ストレス状態を脱するまでの道筋はよく分かっていません。 Hac1の発現により多くの代謝酵素遺伝子群の発現も変動するので、UPRによってさまざまな代謝経路に大きな変化が生じている可能性があります。 UPRを引き起こした細胞をメタボローム解析などに供することを通じ、どのような代謝産物がUPRによって増減し、それがどのように小胞体ストレスの緩和に繋がるか、解明すべく研究を始めています。
ヒトの疾患とUPRとの関わり
ある種の神経変性疾患では、折り畳み不全のタンパク質が発症の原因となります。 サイトゾルに溜まったタンパク質凝集体が小胞体ストレスとなって症状を悪化させる事例も知られています。 私たちの研究室では、神経変性疾患の原因タンパク質を酵母細胞にて発現させ、どのようなメカニズムで小胞体にダメージが与えられるのかも調べています。